《1. 引言》
1. 引言
芳香醛,如苯甲醛,因其在众多领域具有广泛应用,是一类高需求的重要精细化学品[1]。在工业生产过程中,苯甲醛通过甲苯氯化以及随后的皂化获得[2]。此合成过程通常使用强氧化剂,如CrVI、ClO−、Br2或过氧酸,使得目标产物过度氧化,从而导致选择性较低。近年来,随着环境和能源问题的日益突出,以及对能耗大、后处理繁琐、分离困难的工业生产过程不断改善的需求,发展环境友好型的苯甲醛合成工艺迫在眉睫。
近年来,光催化化学反应生成高附加值化学品被认为是一种富有潜力的绿色合成方法,吸引了研究者的关注[3,4]。与传统的热催化相比,太阳能的利用可作为工业生产过程中的潜在能源,从而达到节约能源和保护环境的目的。因此,基于绿色化学和可持续化学的原则,利用半导体将苯甲醇选择性转化为苯甲醛的方法被认为是最具潜力的方法之一。迄今为止,在苯甲醇的氧化反应中已经使用了多种半导体,如金属氧化物、氮化物、硫化物等[1,4–8]。然而,它们大多生产成本高,生产过程对环境不利,选择性差。因此,设计一种新型、经济、高效的用于水相合成苯甲醛的光催化剂具有很大的挑战性。石墨相氮化碳(g-C3N4)具有稳定的物理化学性质、无毒性和适宜的带隙(2.7 eV)等优良特性。此外, g-C3N4可通过各种丰富且廉价的原料获得,如氰胺、尿素、三聚氰胺和硫脲。然而,g-C3N4的光催化活性受限于光生电子(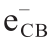 )和空穴(
)和空穴(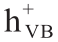 )的快速复合,这使其光催化效率大大降低。将g-C3N4与多种半导体耦合是有效解决上述问题的策略之一[9]。
)的快速复合,这使其光催化效率大大降低。将g-C3N4与多种半导体耦合是有效解决上述问题的策略之一[9]。
多金属氧酸盐(POM)是个庞大且快速扩展的家族,其为过渡金属氧化物团簇。由于POM具有独特的化学结构和与半导体金属氧化物团簇相似的众多特性,通常被认为是后者的类似物,并在各种化学反应中表现出优异的光化学性能[5]。在光的照射下,光催化剂的表面可以捕获光产生的电子和空穴,从而形成·O2−和(或)·OH 自由基的活性物种,进而加速光催化反应。自POM作为催化剂([S2W18O62]4−)[10]用于太阳光照射下催化氧化苯甲醇后,POM在光催化合成高附加值化学品,尤其是芳香醛的合成过程中展现了独特的优势[5,11]。
在本研究中,我们通过将磷钨酸负载于磷酸修饰的g-C3N4表面,成功构筑了一种新型非均相光催化剂(PW12-P-UCNS,其中PW12为H3PW12O40·xH2O,P-UCNS 为磷酸修饰的超薄g-C3N4纳米片),并将该光催化剂应用于绿色光催化反应体系,用于水相选择性光氧化合成苯甲醛。在此催化体系中,制备的PW12-P-UCNS催化剂展现出优异的光催化氧化性能,这归因于以下三点:①引入的POM作为优异的电子受体,能够有效促进光生空穴-电子对的分离;②磷酸的修饰提高了P-UCNS表面催化剂对O2分子的吸附能力,从而有利于在反应过程中生成更多的反应活性物种(·O2−自由基);③PW12-PUCNS的光生电子遵循Z型机理,实现了光生载流子的快速分离。PW12-P-UCNS光催化剂的高氧化活性和可循环使用的特点显示了其广阔的应用前景。
《2. 实验部分》
2. 实验部分
《2.1. 药品和试剂》
2.1. 药品和试剂
所有溶剂和化学品均由上海安耐吉化学有限公司提供,均为分析级,使用时未经进一步处理。
《2.2. UCNS 的合成》
2.2. UCNS 的合成
体相g-C3N4的合成参考文献[12]。将0.9 g体相 g-C3N4分散到150 mL HCl溶液(质量分数为14.8%)中,超声1 h,搅拌24 h,随后在110 ℃下进行水热处理5 h,然后将悬浮液离心、过滤、水洗,最后在80 ℃下烘干过夜,形成无堆叠的g-C3N4纳米片(UCNS)。
《2.3. PW12-P-UCNS 的合成》
2.3. PW12-P-UCNS 的合成
如图1所示,将0.1 g UCNS分散在100 mL 0.3 mol·L−1 的H3PO4溶液中,搅拌5 h,通过离心获得P-UCNS。经 60 ℃干燥180 min后,将样品研磨,并再在300 ℃下焙烧90 min。随即用蒸馏水清洗后干燥,以去除其表面上未结合的磷酸[13]。将一定量的H3PW12O40均匀分散于 20 mL P-UCNS乙醇悬浮液中,持续搅拌。过夜干燥后,最终得到 PW12-P-UCNS光催化剂。
《图1》
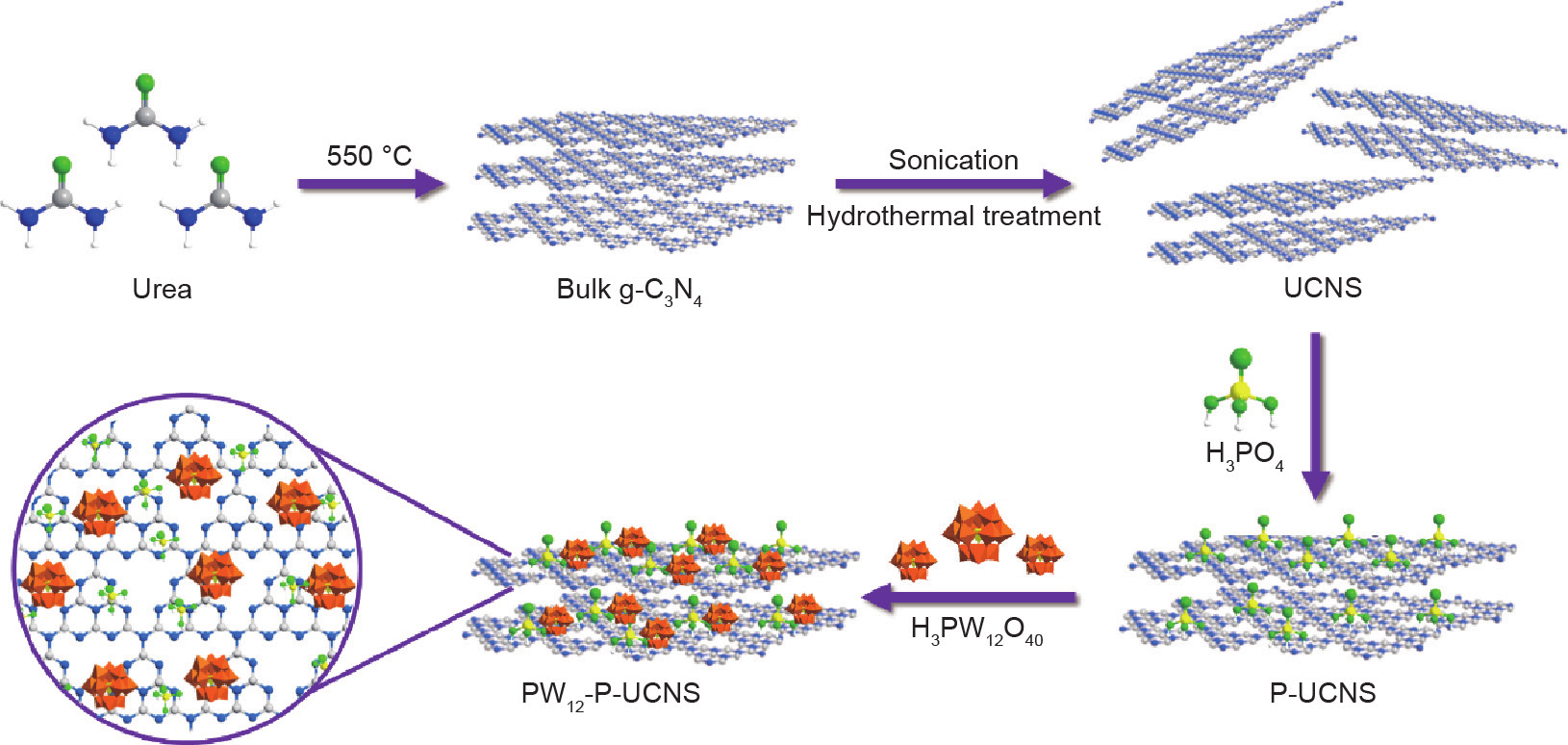
图1. PW12-P-UCNS光催化剂的合成路线。
《2.4. 表征》
2.4. 表征
使用HT7700机器进行透射电子显微镜(TEM)扫描。使用日本岛津公司的XRD-6000衍射仪采集角度为3°~70°的X射线衍射(XRD)光谱图。采用Bruker Vector 22红外光谱仪采集波长为400~4000 cm−1的傅里叶变换红外光谱。采用METTLER TOLEDO(美国)TGA/ DSC 1仪器(SF型,温度最高至1100 ℃)在氮气气氛下进行热重分析(TGA)。使用ULVAC-PHI公司(日本)的Quantera SXM采集X射线光电子能谱(XPS)。使用JEOL JEM-2010型电子显微镜进行高分辨率透射电子显微镜(HRTEM)扫描。孔隙率的测试使用美国 Micromeritics仪器公司的ASAP 2020M仪器进行。
《2.5. 催化性能测试》
2.5. 催化性能测试
选取苯甲醇光氧化反应为模型反应,以300 W氙灯作为光源,在室温条件下系统探究PW12-P-UCNS催化剂的光催化性能。首先,将制备好的20 mg催化剂分散于 10 mL反应物溶液(10 mmol·L−1)中。光照前,将反应体系置于黑暗中持续搅拌30 min,使反应物与催化剂之间达到吸附-解吸平衡。随后,将氧气通入上述混合溶液中并保持光照2 h。结束后,取出1 mL混合物,进行离心、过滤以分离光催化剂。选取环辛烷作为内标物,使用日本岛津公司的GC-2010 Pro气相色谱仪(采用 HP-5色谱柱,色谱柱内径为0.25 mm,长度为30 m)分析产物,并计算苯甲醇的转化率和苯甲醛的选择性。
《2.6. 光电化学测试》
2.6. 光电化学测试
使用CHI 760E电化学工作站(美国CH仪器公司)进行测试,并选择300 W氙灯作为光源。在0.1 mol·L−1 的Na2SO4溶液中进行光电流分析,选择Ag/AgCl和Pt分别作为参比电极和对电极。工作电极的制备方法如下:利用超声将5 mg催化剂均匀分散于1 mL乙醇溶液中。将80 μL上述液体涂于ITO玻璃表面并干燥。循环伏安(CV)图和Mott-Schottky测量方法参考文献[1,12]。
《3. 结果与讨论》
3. 结果与讨论
《3.1. 催化剂合成》
3.1. 催化剂合成
如图1所示,采用水热法和浸渍法成功制备了PW12- P-UCNS催化剂。首先,将尿素在550 ℃下煅烧得到体相g-C3N4。随后,将g-C3N4进行酸处理和超声处理,得到剥离的g-C3N4纳米片。将上述粉末用磷酸进行进一步修饰,并引入PW12,最终得到PW12-P-UCNS催化剂。在此制备过程中,P-UCNS边界的−NH2基团被酸质子化,并在PW12和P-UCNS的界面形成[−NH3+][H2PW12O40− ]物种。由于PW12通过酸碱和静电相互作用负载于P-UCNS,从而避免Keggin基团的流失。此外,引入的PW12加速了载流子的转移和分离。
《3.2. 组成与结构》
3.2. 组成与结构
如图2所示,利用XRD光谱对体相g-C3N4、UCNS、 P-UCNS、PW12和PW12-P-UCNS的化学结构进行探究。在体相g-C3N4的XRD光谱中,位于27.5°和13.0°处的两个宽峰分别对应(002)和(100)晶面[12,14]。由于杂环N原子(C−N=C)的质子化,UCNS和P-UCNS的(002)特征峰与体相g-C3N4相比发生了轻微偏移[15– 17]。此外,P-UCNS的特征峰向更高的2θ角偏移,这是由纳米片之间较低的堆积程度所致[18,19]。在PW12-PUCNS的XRD光谱图中,归属于Keggin结构(2θ = 8°~11°和18°~30°)和P-UCNS(2θ = 14°和28.2°)的特征峰均出现了,表明在引入PW12后,Keggin和P-UCNS的结构均保持不变。
进一步对PW12-P-UCNS催化剂进行傅里叶变换红外光谱(FT-IR)表征以获得其结构信息。在图2(b)中,位于810 cm−1和890 cm−1处的吸收峰来源于庚嗪环的呼吸振动峰[20]。位于1637 cm−1、 1570 cm−1和1463 cm−1处的信号来源于vC−N,而 1416 cm−1处的信号源于vC−N [21,22]。此外,位于 1248 cm−1和1327 cm−1的信号可归属于vC−NH−C或 vC−N(−C)−C [17,23]。位于3000~3500 cm−1处的红外宽峰归属于vO−H和vN−H [24,25]。对于UCNS和P-UCNS催化剂,位于1463 cm−1和1637 cm−1处的信号(分别归属于C=N 和C−N)分别偏移至1466 cm−1和1639 cm−1。此外,位于1570 cm−1处的CN杂环中的C=N信号峰强度明显降低,表明g-C3N4已成功质子化[15,26,27]。P-UCNS催化剂在985 cm−1处出现了新的特征峰,其归属于磷酸基团[28]。PW12分别在1080 cm−1、984 cm−1、890 cm−1 和798 cm−1处出现特征振动峰[29]。PW12和P-UCNS的上述所有特征峰均在PW12-P-UCNS的FT-IR光谱图中出现。因此,上述的结果说明:① g-C3N4经过剥离、质子化、磷酸改性后成功转化为P-UCNS;② PW12成功负载于P-UCNS表面;③ PW12的Keggin结构在负载后仍然保持完整。
《图2》
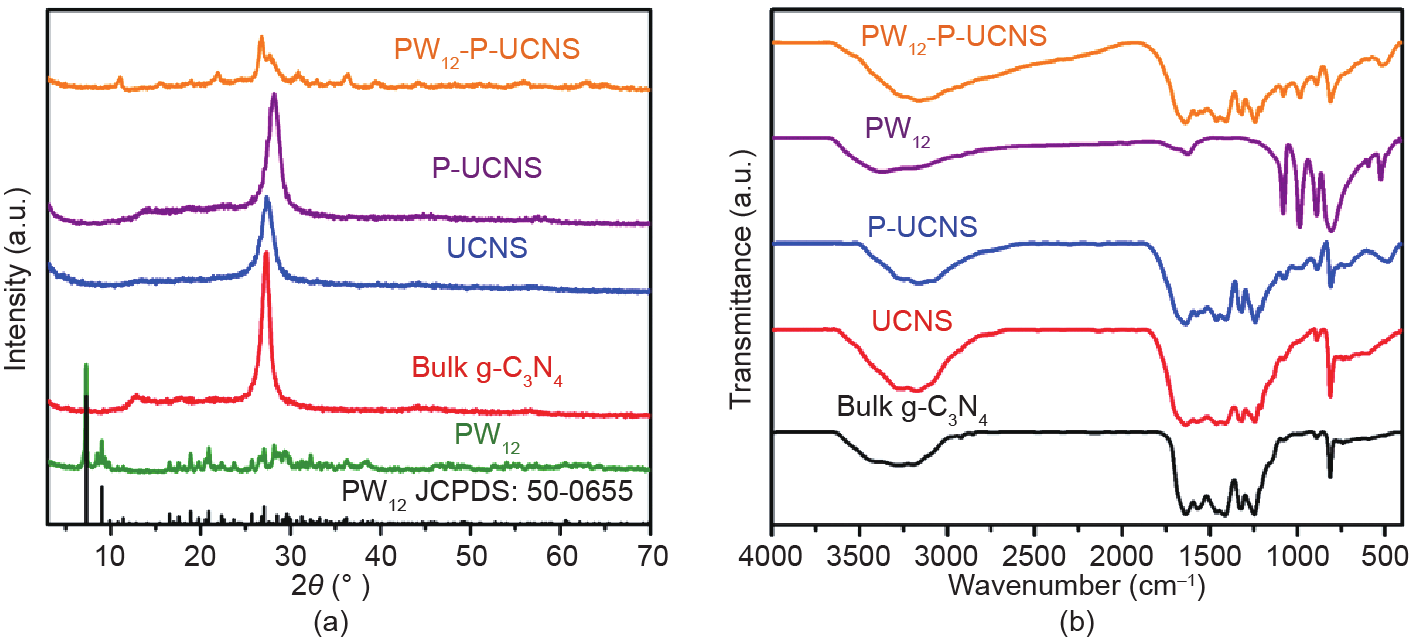
图2. UCNS、P-UCNS、体相g-C3N4、PW12和PW12-P-UCNS的XRD光谱图(a)和FT-IR光谱图(b)。
随后,将PW12-P-UCNS催化剂进行XPS表征。如图3(a)所示,P、O、N、W和C元素的信号峰清晰可见。PW12-P-UCNS催化剂的C 1s XPS光谱图[图3(b)] 可被拟合为289.2 eV、288.0 eV、286.0 eV和284.8 eV处的4个特征峰。其中,结合能位于288.0 eV和284.8 eV处的特征峰分别归属于N=C(−N)2单元和石墨相中的不定形碳[16,30,31]。以C−O和C−NH2形式存在的碳原子分别位于图中的289.2 eV和286.0 eV处。在N 1s光谱图中 [图3(c)],位于404.0 eV、400.2 eV、399.1 eV和 398.2 eV处的4个特征峰分别归属于C−NH+ =C、C−N−H 或N−H2基团、N−(C)3和sp2 杂化的C−N=C基团[32–35]。此外,由于质子化和PW12物种的强静电相互作用, PW12-P-UCNS催化剂的C 1s和N 1s光谱图中的特征峰与 UCNS和P-UCNS相比均发生了明显偏移[13,17,29]。在图3(d)中,从PW12-P-UCNS催化剂的W 4f XPS光谱图中可看到位于37.4 eV和35.3 eV处的两个特征峰,分别归属于W 4f5/2和W 4f7/2自旋轨道,表明引入的PW12中的W元素为WVI物种[36]。另外,从图中还能发现PW12- P-UCNS催化剂中的这两个特征峰的位置相比PW12光谱图(W 4f5/2为37.9 eV和W 4f7/2为35.8 eV)向低结合能方向发生偏移,这是由于P-UCNS与Keggin基团之间存在较强的化学作用[37]。
《图3》
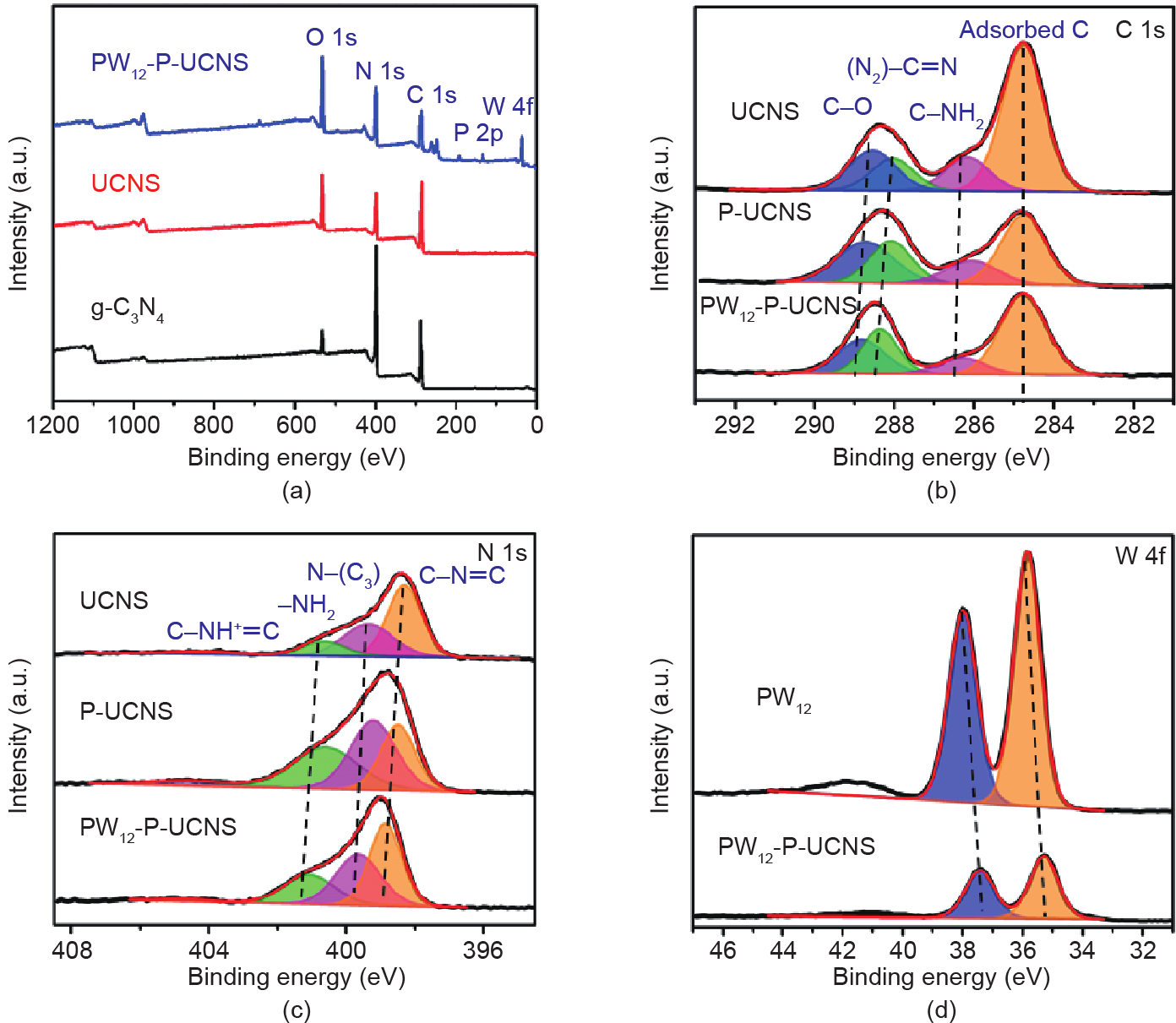
图3. 不同催化剂(PW12-P-UCNS、g-C3N4和UCNS)的XPS光谱图(a);UCNS、P-UCNS、PW12-P-UCNS的C 1s XPS光谱图(b)和N 1s XPS光谱图(c)以及PW12和PW12-P-UCNS的W 4f XPS光谱图(d)。
《3.3. 形貌与性质》
3.3. 形貌与性质
PW12-P-UCNS的形貌用TEM进行探究,并与g-C3N4、 UCNS和P-UCNS进行比较。如图4所示,所制备的材料均呈现纳米层状结构。与呈现较厚块状结构(厚度约为29 nm,见附录A中的图S1)的g-C3N4相比,制备的PW12-P-UCNS为超薄纳米片(厚度约为12 nm,见图 S1)。开放的表面提供了丰富的活性位点和更短的传质距离,有利于加速电荷的分离与转移,从而增强PW12- P-UCNS的光氧化活性[38]。此外,g-C3N4经水热处理后,UCNS的厚度迅速下降至10 nm,并且,在引入磷酸和POM后厚度依然保持不变,这一结果与原子力显微镜(AFM)得到的结果一致。仔细观察HRTEM图像(见附录A中的图S2)发现,PW12-P-UCNS中有许多均匀分散的黑点,其尺寸与PW12团簇一致,说明PW12- P-UCNS中的多酸分子呈黑点状均匀分布于P-UCNS上。此外,通过孔隙率表征证明UCNS、P-UCNS和PW12-PUCNS具有多孔的纳米结构(见附录A中的图S3)。
《图4》

图4. PW12-P-UCNS(a)、P-UCNS(b)、UCNS(c)和体相g-C3N4(d)的TEM图。
《3.4. 光谱吸收性质》
3.4. 光谱吸收性质
利用紫外-可见漫反射光谱(UV-Vis/DRS)探究 UCNS、g-C3N4、P-UCNS和PW12-P-UCNS的能带结构和光学吸收特性。如图5所示,PW12的吸收区域为 200~422 nm,这是由W=O和W−O−W处的O 2p到W 5d轨道的电荷转移造成的[12]。此外,其余催化剂的吸收边为440~480 nm,这是由电荷从N 2p轨道的价带(VB)跃迁到C 2p轨道的导带(CB)所引起的[39]。在PW12- P-UCNS催化剂的光谱中未发现与PW12或P-UCNS相关的吸收峰(图5),表明负载的PW12均匀分散于催化剂中[13]。依据(αhv) 1/2相对光子能(hv)的变化图(见图S4),按照公式(αhv) 1/2 = A (hv – Eg)计算催化剂的带隙(Eg),式中,v、Eg、A和α分别代表光的频率、带隙能量、比例常数和吸收模量[40,41]。PW12、g-C3N4、 UCNS和P-UCNS的Eg分别为2.80 eV、2.62 eV、2.69 eV 和2.42 eV。相比于g-C3N4和UCNS,带隙能的蓝移证明 P-UCNS的光吸收能力有所提高。
《图5》
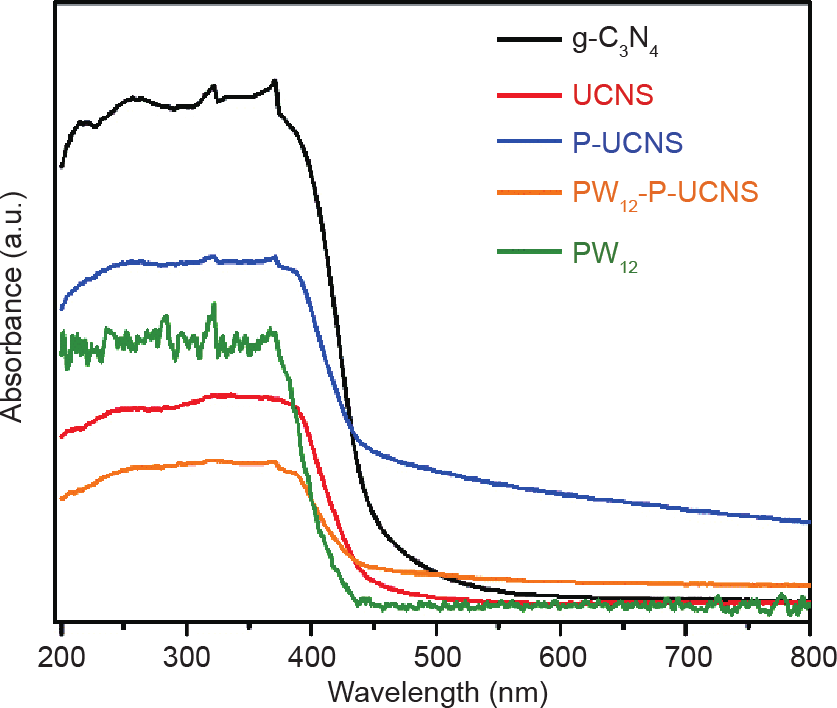
图5. g-C3N4、UCNS、P-UCNS、PW12和PW12-P-UCNS的紫外-可见漫反射吸收光谱图。
《3.5. 催化性能》
3.5. 催化性能
以氙灯作为反应光源,选取在水相中氧化苯甲醇来探究PW12-P-UCNS的光催化性能。作为对比,同时探究了PW12、P-UCNS和不同PW12负载量的PW12-P-UCNS催化剂的光催化性能(相应的表征结果如图S5和S7所示)。
图6(a)显示了PW12、P-UCNS和PW12-P-UCNS在氙灯照射下对苯甲醇选择性氧化的活性。在相同的条件下,还进行了不添加光催化剂的空白对照实验,结果表明,不添加PW12-P-UCNS的反应在照射2 h后几乎无法进行。针对反应物苯甲醇与光催化剂之间存在的吸附平衡问题,首先将催化体系置于黑暗中并匀速搅拌0.5 h。光照2 h后,光催化氧化活性的顺序为:PW12-P-UCNS > P-UCNS > PW12。结果表明,PW12-P-UCNS具有最高的光催化氧化活性,苯甲醇转化率为58.3%,苯甲醛选择性为99.5%。此外,探究了不同PW12负载量对PW12-PUCNS催化性能的影响。如图6(b)所示,随着PW12负载量的增加,苯甲醇的转化率上升,而苯甲醛的选择性明显降低。综合考虑苯甲醇的转化率和苯甲醛的选择性,选取PW12负载量为34.8%(质量分数)的PW12-PUCNS进行后续的光催化性能测试(见图S8)。进一步将制备的PW12-P-UCNS的光催化氧化活性与文献中报道的活性进行比较,结果显示,其展现出优异的催化性能(见表S1)。制备的PW12-P-UCNS催化剂具有以下三个方面的优势:①催化体系的溶剂为水,合成过程绿色、环境友好并可持续发展;②在温和的反应条件下(反应时间短、反应温度低)获得高选择性目标产物和高转化率反应物;③与贵金属相比,该催化剂稳定性高,生产成本低。
《图6》
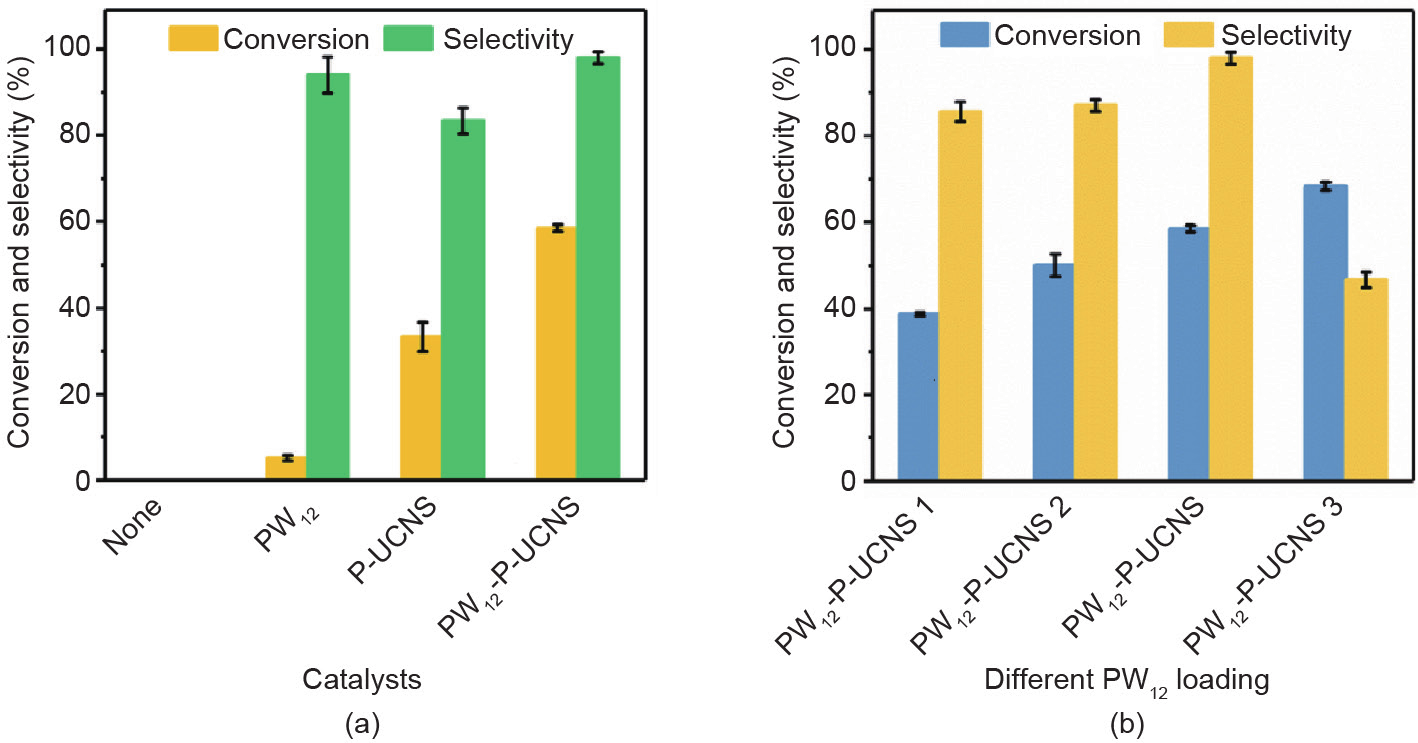
图6. 不同光催化剂(a)和不同PW12负载量(b)的PW12-P-UCNS在水相中的苯甲醇转化率和苯甲醛选择性。PW12-P-UCNS的PW12负载量为 34.8%(质量分数);PW12-P-UCNS 1的PW12负载量为13.7%(质量分数);PW12-P-UCNS 2的PW12负载量为22.6%(质量分数);PW12-P-UCNS 3 的PW12负载量为46.2 %(质量分数)。反应条件:20 mg催化剂,10 mL水,0.1 mmol苯甲醇,氙灯照射2 h。
《3.6. 光催化剂的循环利用》
3.6. 光催化剂的循环利用
光催化剂的再生性和重复使用性是评价其性能的两个关键问题。在本研究中,将制备的PW12-P-UCNS催化剂用于催化苯甲醇的氧化反应,并连续循环5次。如图7 (a)所示,连续5次循环后,苯甲醛的选择性基本保持不变,而苯甲醇的转化率在3次循环后略有下降。为了分析活性损失的原因,首先将光催化剂与反应液分离,并进行电感耦合等离子体原子发射光谱(ICP-AES)分析,以确定PW12是否在催化体系中浸出。钨含量的结果表明,反应过程中没有磷钨酸溶脱现象发生。此外,通过FT-IR、XRD和TEM等表征手段对回收的PW12-PUCNS催化剂的结构和形貌进行研究。如图7(b)所示,回收的PW12-P-UCNS催化剂仍然保持薄的纳米片结构。此外,在图7(d)中,仍可清晰观察到归属于PW12的 Keggin结构的特征峰,说明PW12-P-UCNS未发生明显的结构变化。以上结果表明,进行连续5次循环实验后, PW12-P-UCNS的活性降低可能是由于循环实验过程中催化剂的质量损失引起的,并且所制备的PW12-P-UCNS可以连续进行至少5次循环使用,同时不发生明显的形貌和结构变化。
《图7》
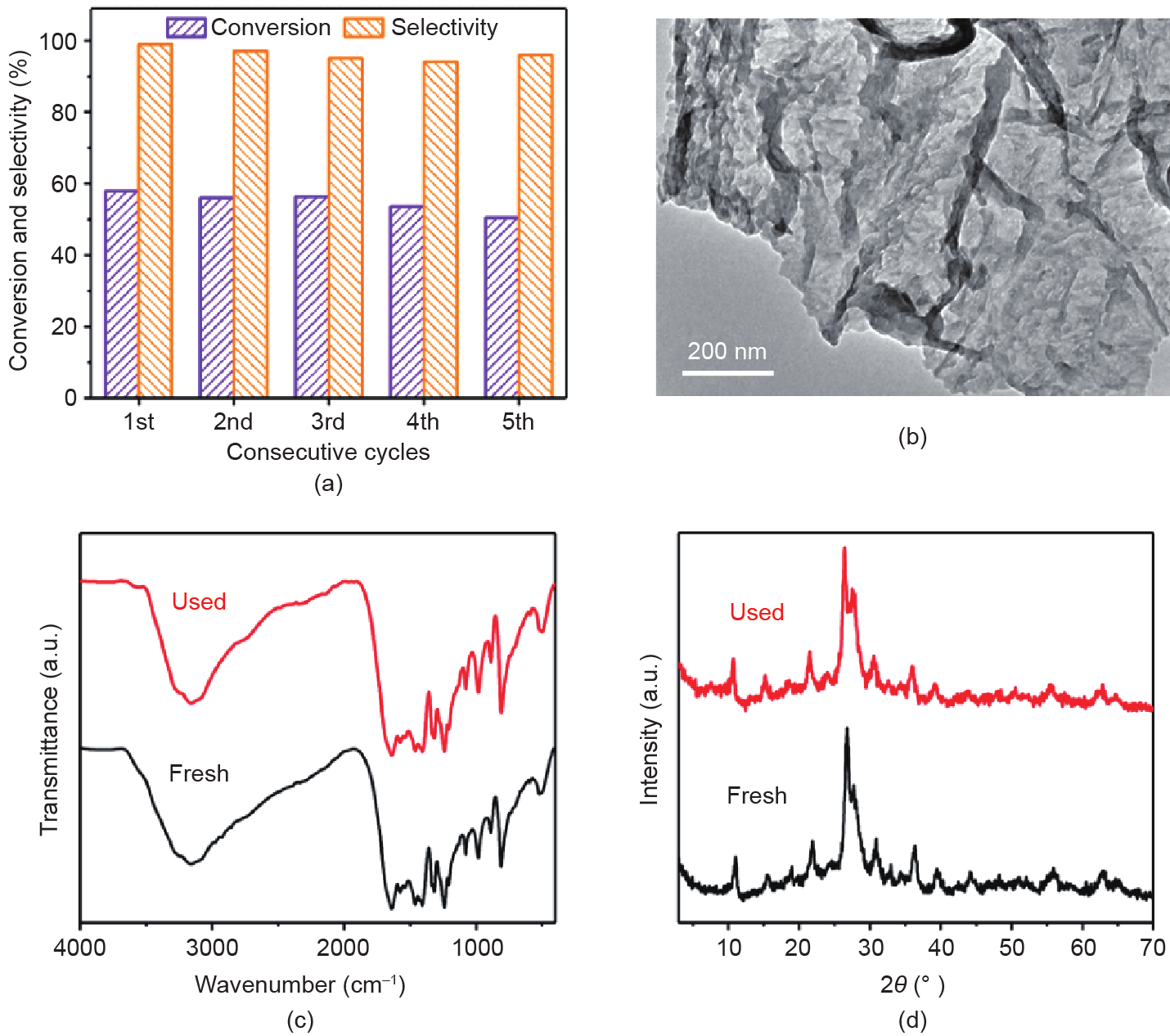
图7. PW12-P-UCNS催化剂的催化循环性能图(a)、PW12-P-UCNS催化剂使用前后的TEM图(b)、FT-IR光谱图(c)和XRD光谱图(d)。反应条件:20 mg催化剂,10 mL水,0.1 mmol苯甲醇,氙灯照射2 h。
《3.7. 光催化机理》
3.7. 光催化机理
光催化反应中电荷分离和电子转移的效率可以通过测试光电化学性能来监测[4]。首先,利用瞬态光电流测试评价所制备的P-UCNS和PW12-P-UCNS光催化剂光生载流子的分离和转移效率。如图8(a)所示,P-UCNS 和PW12-P-UCNS的光电流响应可以在5个光照周期内重现并保持稳定。PW12-P-UCNS催化剂的光电流强度(2.52 μA)是P-UCNS(0.66 μA)的3.8倍,表明在催化体系中引入PW12能够在一定程度上提高光生载流子的分离和转移能力。引入的PW12作为优异的电子受体有效限制了光生电子和空穴的复合。此外,光致发光(PL)光谱反映了光生电子-空穴对的复合速率。如图S9所示,制备的PW12-P-UCNS催化剂相比g-C3N4、UCNS和 P-UCNS具有最低的光生载流子复合率,这与瞬态光电流的测试结果一致。
随后,利用电化学阻抗谱(EIS)对光生电子和空穴的分离效率进行研究[2]。电荷转移和分离效率可以通过Nyquist图的半圆半径大小来反应,半圆的半径越小则电荷转移阻抗越小,光生电子的转移能力越强 [42,43]。相比P-UCNS,PW12-P-UCNS催化剂显示出直径更小的半圆,这意味着PW12-P-UCNS具有更小的光电阻抗和更高的电荷分离效率[图8(b)]。上述结果表明, PW12的引入有效提高了光催化剂的光生载流子分离和转移效率。
《图8》
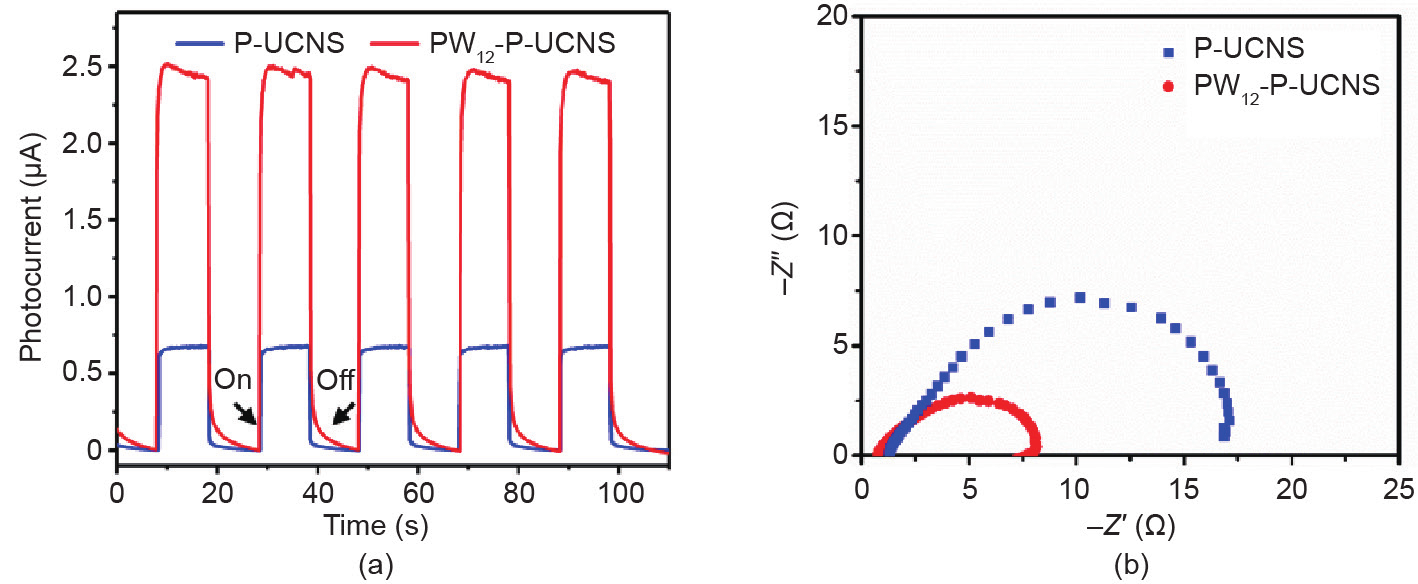
图8. P-UCNS和PW12-P-UCNS的瞬态光电流图(a)与电化学阻抗谱(EIS)(b)。–Z′′:虚部阻抗;Z′:实部阻抗。
为了探究PW12-P-UCNS催化剂选择性苯甲醇氧化反应的机理,借助电子自旋共振(ESR)来监测苯甲醇氧化过程中可能形成的活性物质。如图9(a)所示,在无光照的条件下未出现特征峰信号。在光照条件下,在存在PW12-P-UCNS催化剂的甲醇溶液体系中,出现了强度比为1∶1∶1∶1的四重特征峰,将其归属于5,5-二甲基-1-吡咯啉氮氧化物(DMPO)-·O2−的特征峰[44]。这表明PW12-P-UCNS催化剂在光照反应过程中有超氧自由基(·O2−)生成。
使用过硫酸钾(K2S2O8)作为电子捕获剂、草酸(C2H2O4)作为空穴捕获剂、1,4-苯醌(BQ)作为·O2−捕获剂以及叔丁醇(TBA)作为·OH捕获剂[1,2,5,45],仔细考察了不同活性物质对模型反应的影响。如图9(b)所示,当在反应体系中加入C2H2O4或BQ时,苯甲醇转化率急速下降,这一结果证明了·O2−和空穴是该反应体系中重要的活性物质。然而当加入TBA后,反应底物苯甲醇的转化率未发生明显改变,这一结果说明·OH对于该反应体系无重要作用。此外,在添加K2S2O8之后,苯甲醇的转化率略有上升,这可能是由于电子捕获剂的添加增加了对光生电子的消耗,从而导致PW12-P-UCNS上光生空穴数量的增加,使得空穴将催化剂表面的苯甲醇氧化,提高了转化率[1]。
《图9》
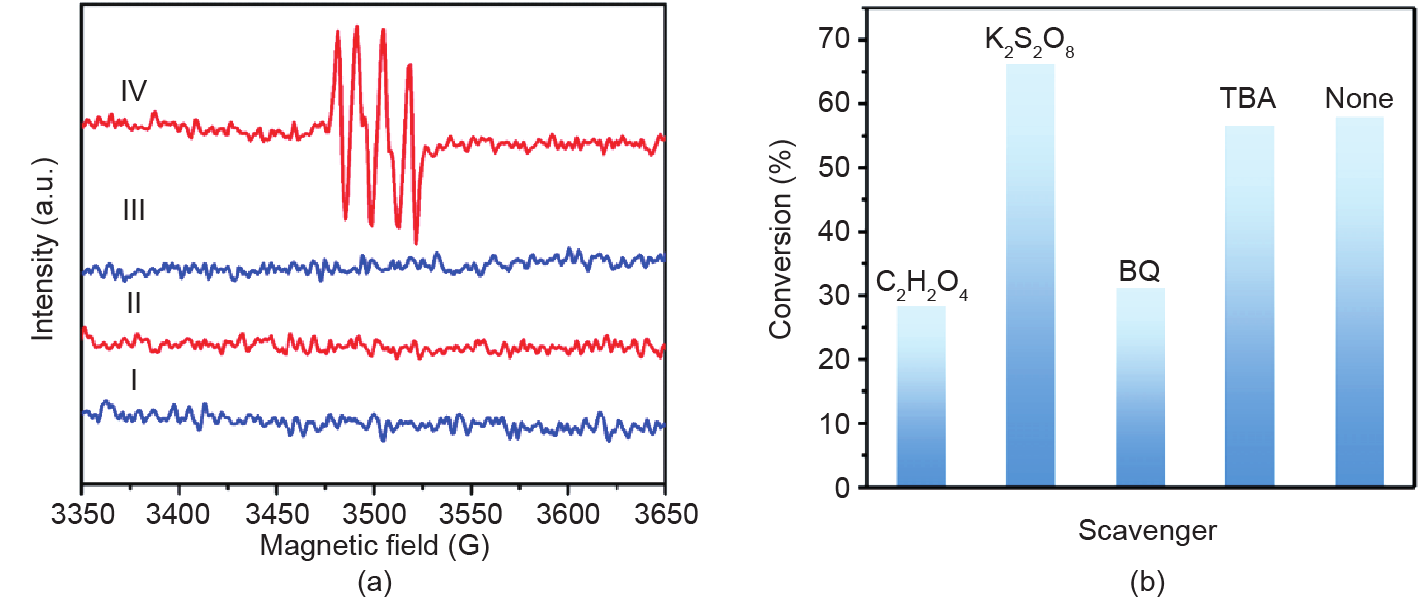
图9. (a)PW12-P-UCNS的ESR图。I:DMPO在黑暗条件下;II:PW12-P-UCNS在黑暗条件下;III:DMPO在氙灯照射下;IV:PW12-P-UCNS在氙灯照射下。(b)PW12-P-UCNS光催化的苯甲醇氧化反应中活性物质的捕获实验。1 G = 1 × 10−4 T。
基于上述结果,在PW12-P-UCNS光催化的苯甲醇氧化反应中,光生空穴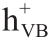 和·O2−是主要的活性物质。
和·O2−是主要的活性物质。
通过计算催化剂的带隙、CV曲线和测量平带电势(见图S10),估算出PW12和P-UCNS的CB和VB的相对位置。基于以上结果,可能的反应机理为传统的II型异质结机理或者Z型机理。
如果制备的PW12-P-UCNS催化剂遵循II型-异质结机理,则P-UCNS的CB中的光生电子会在PW12的未占有电子的能级最低的轨道(LOMO)中积累,而PW12 的VB中的空穴会转移到P-UCNS的已占有电子的能级最高的轨道(HOMO)。如图S11所示,PW12的CB的电势(+0.30 V vs NHE,由CV法测定,NHE是标准氢电极,见图S10)比O2/·O2−的氧化还原电势(−0.33 V vs NHE)更正[28,46],这很难将O2直接还原为·O2−。同理, P-UCNS的VB上的空穴也无法生成·O2−。上述提出的II 型-异质结机理与ESR结果相矛盾。因此,对于该催化体系,我们提出了Z型机理。
图10揭示了PW12-P-UCNS选择性光催化苯甲醇氧化合成苯甲醛的机理。PW12-P-UCNS受到光照激发后,形成了光生空穴-电子对[式(1)]。PW12和P-UCNS紧密接触并且二者的能带结构匹配良好,这促使P-UCNS 的VB会连续不断接收来自PW12 CB上自发迁移的光生电子,PW12的光生电子与P-UCNS的空穴发生复合。在 Z型机理驱使的苯甲醇光氧化反应中,PW12 VB的空穴将反应底物苯甲醇氧化为自由基阳离子C6H5CH2OH*+ [式(2)]。同时,由于磷酸的修饰使得P-UCNS表面能吸附更多的O2 [13,28,46],O2捕获P-UCNS的电子后产生更多的·O2− [式(3)]。最终,·O2−与自由基阳离子 C6H5CH2OH*+ 反应生成目标产物苯甲醛[式(4)]。
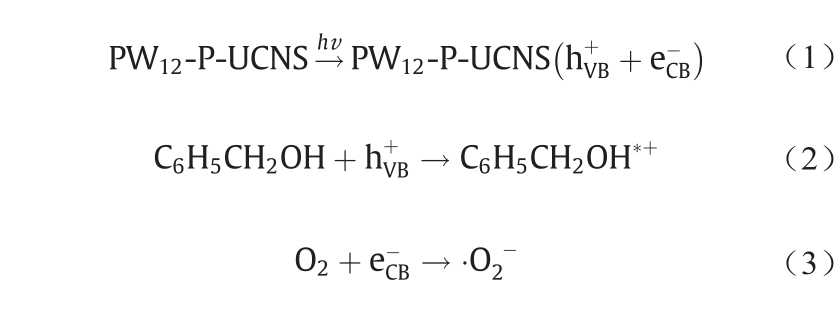
《图10》
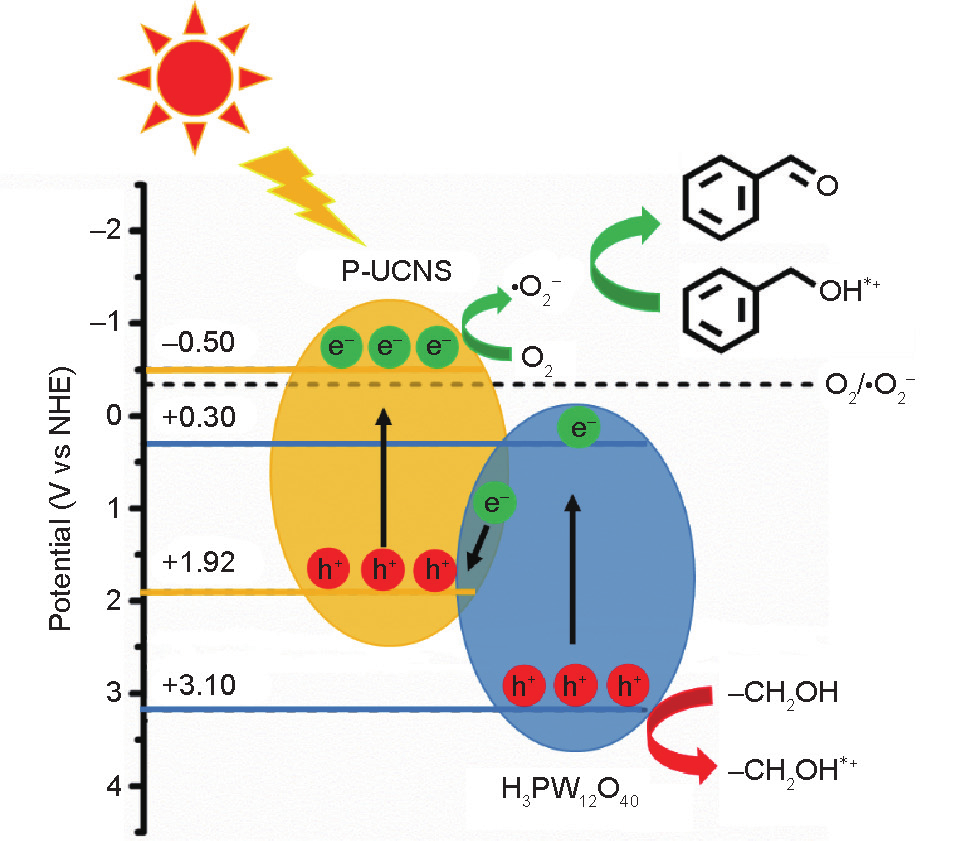
图10. 水相中PW12-P-UCNS光催化选择性氧化苯甲醇的反应机理。
另一方面,由于PW12-P-UCNS光催化剂表面存在 C−N−H、C−OH和POM物种,因此其可以作为氢键受体。因此,PW12-P-UCNS光催化剂表面更易通过氢键或静电相互作用吸附反应物,从而获得较高的苯甲醇转化率。同时,苯甲醛与PW12-P-UCNS之间的弱相互作用使得前者能迅速从表面解吸,避免了目标产物的过度氧化,从而获得了苯甲醛的高选择性。该Z型机理驱使的光催化氧化反应表现出优异的苯甲醇转化率和苯甲醛选择性,这归因于光生电子-空穴对的快速分离和大量的·O2−。基于上述结果,所制备的PW12-P-UCNS对于水相中苯甲醇的氧化反应是高效、环境友好的光催化剂。
《4. 结论》
4. 结论
综上所述,通过将PW12负载于磷酸修饰的g-C3N4 纳米片上,成功构建了一种高效、环境友好型PW12-PUCNS光催化剂。所制备的PW12-P-UCNS光催化剂在选择性氧化苯甲醇合成苯甲醛的反应中表现出优异的光催化性能,即反应2 h后,苯甲醇转化率为58.3%,苯甲醛选择性为99.5%。通过光电流测试、自由基捕获实验和 ESR表征等光化学性质的测定,提出Z型光催化机理。 PW12-P-UCNS光催化剂的优异性能可归因于以下几个方面:①引入的Keggin基团有效促进了电子的自发迁移,从而加速了载流子的分离;②P-UCNS表面吸附更多的 O2,从而产生更多的·O2−(当前选择性光氧化反应过程中的主要活性物种)。基于上述结果,PW12-P-UCNS光催化剂在光驱动的氧化反应中表现出巨大潜力。
《致谢》
致谢
本研究受国家自然科学基金(21625101、21521005 和21808011)、国家重点研发计划(2017YFB0307303)、北京市自然科学基金(2202039)和中央高校基金(XK1802-6、XK1902和12060093063)资助。
《Compliance with ethics guidelines》
Compliance with ethics guidelines
Lifu Wu, Sai An, and Yu-Fei Song declare that they have no conflict of interest or financial conflicts to disclose.
《Appendix A. Supplementary data》
Appendix A. Supplementary data
Supplementary data to this article can be found online at https://doi.org/10.1016/j.eng.2020.07.025.













 京公网安备 11010502051620号
京公网安备 11010502051620号




