《1 前言》
1 前言
自从19世纪工业革命以后, 大气中的CO2浓度开始迅速上升, 到了20世纪后半叶, 这一趋势进一步加剧。CO2的排放主要来源于能源、交通、工业等部门大量化石燃料的燃烧
为了减轻化石燃料燃烧对环境造成的冲击, 近年来一些发达国家和能源公司开始从事化石燃料燃烧过程中CO2的捕集和安全封存技术。目前研究较多的CO2捕集技术主要有燃烧后分离技术 (post-combustion scrubbing) 、燃烧前脱碳技术 (pre-combustion decarbonization) 和纯氧燃烧技术 (oxyfuel) 。燃烧后分离技术就是在化石燃料燃烧后的烟道中采用物理或化学的方法使CO2矿物化生成稳定的物质固定下来, 或使CO2 从烟气中分离出来, 得到高纯度的CO2然后封存;燃烧前脱碳技术就是在燃料燃烧以前使燃料重整改质, 先生成CO2和H2, 把CO2分离后用洁净的氢能供热或发电;纯氧燃烧技术就是在燃烧之前把助燃空气中的O2和N2分离, 用纯氧来进行燃烧, 则燃烧后的废气只有CO2和水蒸气, CO2很容易和水蒸气分离, 然后进行封存。但是, 由于存在工艺比较复杂及成本过高等问题, 目前都未获得广泛应用, 特别是在发展中国家。为了减少化石燃料燃烧带来的大气污染问题, 近年来国内外许多工程技术人员都在致力于开发高效节能、低污染排放的燃烧技术, 如高性能蓄热燃烧技术、高温低氧燃烧技术和受控脉动燃烧技术等。这些技术在很大程度上节约了能源、降低了污染排放, 但都不能从根本上解决化石燃料燃烧的污染问题。为了最大限度地减小化石燃料燃烧对环境造成的压力, 笔者提出了熔融盐循环热载体无烟燃烧技术。
《2 NFCT的技术路线》
2 NFCT的技术路线
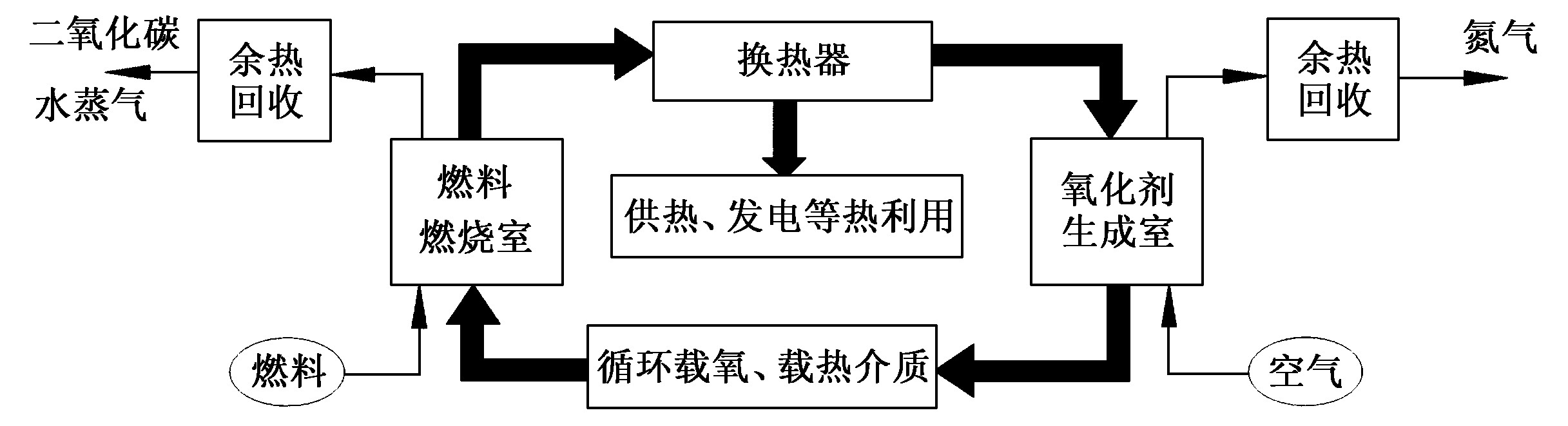
图1为熔融盐循环热载体无烟燃烧技术的流程图
特点是将燃料与助燃空气的燃烧分为氧化剂的生成和燃料与氧化剂反应两个过程, 并且两个过程分别在两个反应器中进行。该燃烧技术的第一部分是氧化剂生成室。这一步在一个反应器里进行, 反应器里充满了熔融盐, 氧化物或其它载氧介质分散在熔融盐里, 空气被空压机或风机鼓入溶池中, 当氧气接触到氧化物时, 即和氧化物发生作用, 生成更高价的氧化物, 氧元素以化合物的形式被吸收在体系内。这一步若控制好反应条件和空气流速, 空气中氧气能完全被氧化物结合, 而只剩下氮气, 较纯的氮气则被回收用作商品。第二部分, 熔融盐和氧化物被传输到另一个反应器, 这部分称为燃料燃烧室。在这一反应器里, 燃料被送入熔池中与氧化物反应, 氧化物把在第一步里得到的氧传递给燃料, 燃料和氧化物发生氧化还原反应, 若控制好燃料的供给量, 二者能刚好完全反应, 那么燃烧产物中只有CO2和水蒸气, CO2很容易从水蒸气中分离回收, 这一步也不向大气中排放有害气体。最后, 储存了大量热量的熔融盐热载体在换热器里进行热交换, 热量被传到其它介质用于发电或供热。由燃烧过程可以看出, 熔融盐和氧化物在整个过程中分别起到了热载体和氧载体的作用, 熔融盐反复地吸热和放热, 实现热利用;氧化物不断地在氧化剂生成室得氧和在燃烧室失氧, 完成燃烧过程。在氧化剂生成室氧气和氮气被分离, 氮被回收, 在燃烧室因为没有氮气存在而避免了NOx的生成, 只生成了CO2和水蒸气, CO2也可回收利用, 因而整个燃烧过程不向大气排放有害气体。
《3 试验过程与方法》
3 试验过程与方法
本试验在一个单体反应器中进行, 试验装置如图2所示。
反应器尺寸为ϕ120 mm×480 mm, 材质为不锈钢;采用的熔融盐体系为1∶1∶1的Li2CO3+K2CO3+Na2SO4, 催化剂采用CuO。整个反应器置于一个自动控温的管式电炉中加热, 电炉温度控制在750℃, 待反应器中的温度升到750℃后, 各种盐已完全熔融, 鼓入空气把物料完全混合均匀后取样进行XRD分析;然后向熔池中通入CH4气体, 使CH4和熔池中的CuO和Na2SO4发生氧化还原反应, 并对反应后的烟气成分进行分析, 待反应器中的CuO和Na2SO4被全部还原成Cu2O和Na2S后, 向反应器中通入空气和新生成的Cu+和S2-发生反应, 重新生成CuO和Na2SO4。
《4 结果与讨论》
4 结果与讨论
《4.1热力学分析》
4.1热力学分析
在燃料燃烧室和氧化剂生成室进行的化学反应分别如下:
燃烧室:
氧化剂生成室:
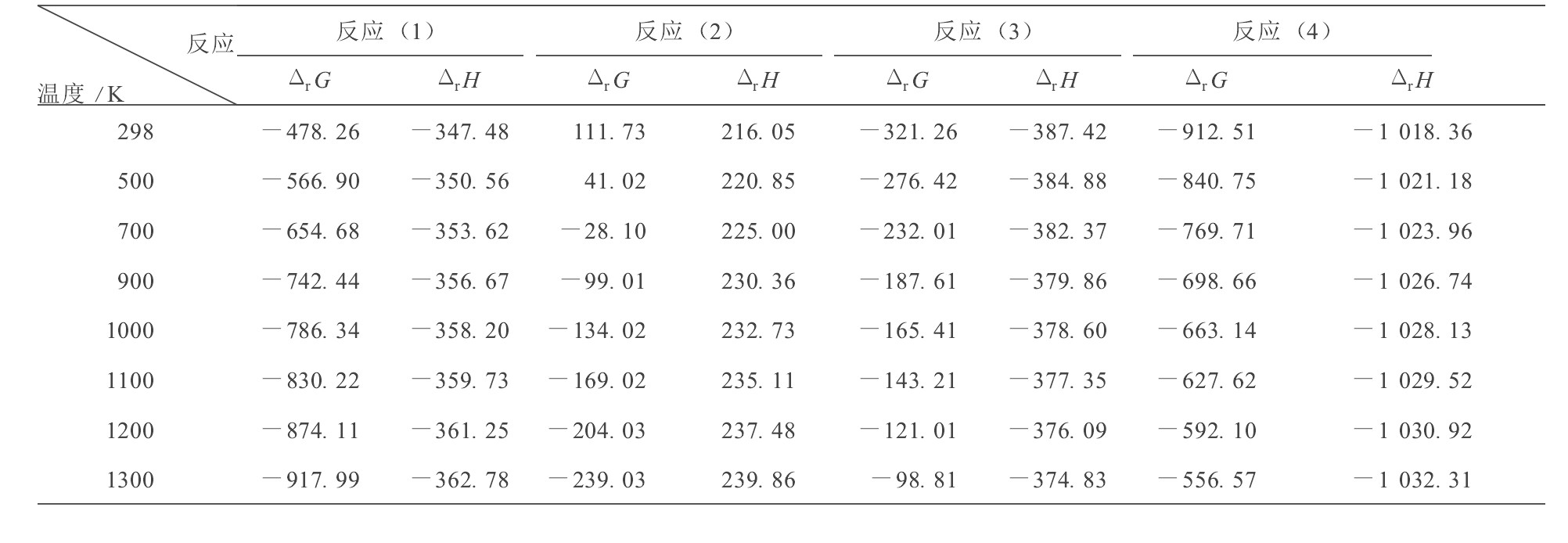
反应 (1) 至 (4) 在不同温度下的吉布斯自由能ΔrG和焓变ΔrH列于表1。热力学计算表明, 以上4个反应的ΔrG在一个很宽的范围内都是小于零的, 说明以上反应在通常的燃烧温度下是可以自发地向右进行。由表1可知, 反应 (1) ~ (4) 中, 除了反应 (2) 以外其余3个反应均为放热反应。如果令反应 (1) +2 (3) 或者反应 (2) + (4) 就可以得到如下同一个反应:
由此可知, 虽然无烟燃烧技术把燃烧过程分为两个步骤进行, 但令两个步骤迭加, 得到整个燃烧过程的总反应方程仍是传统的燃烧过程反应。因此, 如果燃烧反应进行完全, 整个燃烧过程放出的热量可根据过程消耗的CH4或空气量按反应 (5) 的焓变ΔrH进行计算。
表1反应 (1) 至 (4) 的ΔrG和焓变ΔrH 的计算结果 (kJ/mol)
Table 1 The ΔrG and ΔrH of reactions (1) through (4) at different temperatures (kJ/mol)
《图3》
《4.2反应产物气体成分气相色谱分析》
4.2反应产物气体成分气相色谱分析
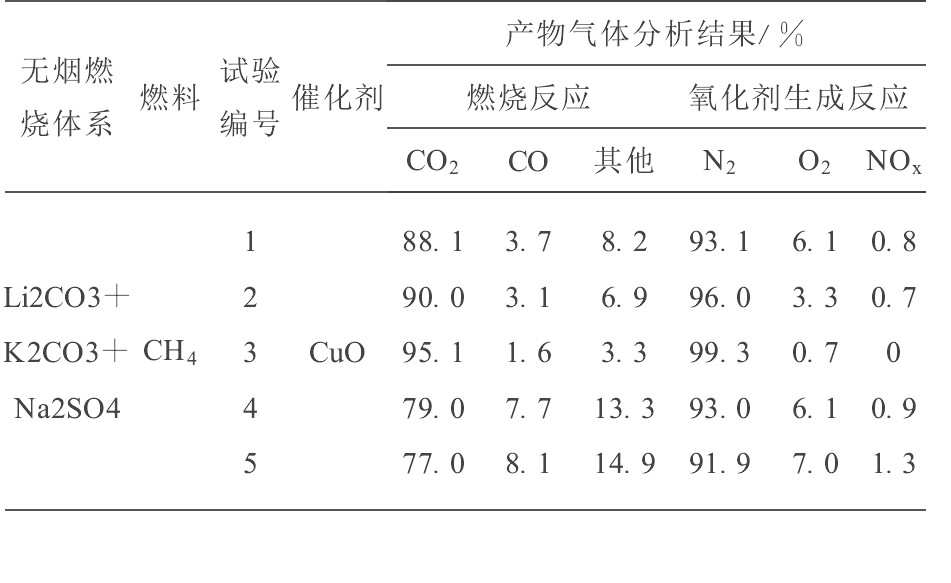
如果反应器里的实际反应按着热力学分析的过程进行, 在CH4通入溶池反应后的尾气主要成分应为CO2, 而在氧化剂生成反应后的气体应是高纯度的N2。表2是色谱分析的试验结果。
由色谱分析结果显示, 燃烧反应后的产物气体主要由CO2组成, 试验测得的结果w (CO2) 的质量分数为77.0%~95.1%之间。据此可以推断, 在燃烧反应过程中, CH4和熔融盐体系中的Na2SO4或CuO发生了反应, 即反应朝着热力学分析的方向进行, 同时还生成了Cu2O 和 Na2S。但如果反应过程严格按照反应 (1) 和 (2) 的情形进行, 则产物气体中应没有CO, 而实际检测的结果是产物气体中存在CO。很显然, 实际反应过程要远比热力学分析的结果复杂。产生CO的原因可能是由于CH4被Na2SO4或CuO部分氧化的结果, 其他可以检测到的气体有未反应的CH4, H2等。虽然燃烧反应没有像理论分析的那样得到完全的CO2气体, 但在这个无烟燃烧体系下能得到90%以上纯度的CO2气体, 非常有利于CO2的捕集和封存, 对减少温室气体的排放具有重要意义。
由表2还可以看出, 在氧化剂生成反应后的气体产物中是纯度高的N2, 其质量分数达到了91.9%~99.3%。这说明在氧化剂生成反应中, 空气中的氧气和熔融盐体系中Cu2O和Na2S (上一步的反应产物) 发生了反应。根据试验结果, 产物气体中还存在0.7%~7.0%的氧气及少量的NO2等氮氧化物。熔融盐循环热载体无烟燃烧技术是新近才提出并开始研究的新技术, 其中还存在许多问题需要进一步深入研究, 如反应过程动力学、热利用、熔融盐安全性、反应速率等。
《4.3XRD分析结果》
4.3XRD分析结果
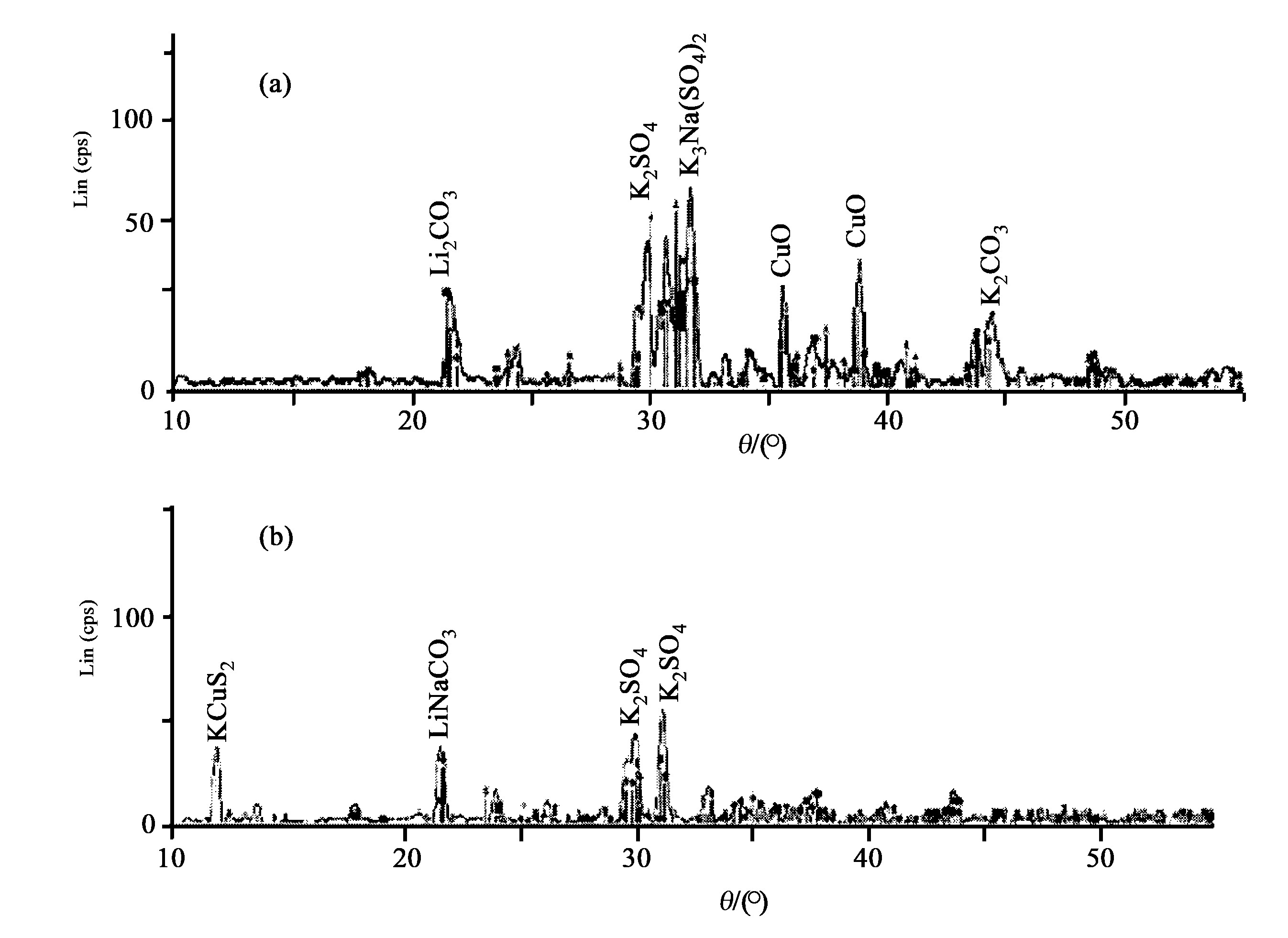
图3中 (a) 与 (b) 分别为CH4与熔融盐体系反应前后的XRD分析结果图谱。
X衍射分析结果显示, CH4通入熔池之前, XRD检测出的主要成分有Li2CO3, K3Na (SO4) 2, CuO, K2SO4 和 K2CO3等物质。可见, 尽管初始加入反应器的原料为Li2CO3, K2CO3, Na2SO4和CuO, 但经过熔融以后, 因为熔融盐中各种物质是以离子态存在的, 熔盐体系中各离子发生了重新组合, XRD检测到的是重新组合后的物质形态, 但各元素的价态没有发生变化, 说明此时熔池中没有发生氧化还原反应。向熔池中通入CH4使其与熔融盐发生作用以后, XRD检测出的主要成分有LiNaCO3, K2SO4和KCu3S2。理论上, CH4与熔池中的Na2SO4和CuO发生反应后应该生成Cu2O和Na2S, 但熔融盐中各离子之间的作用非常复杂, 新生成的物质容易和其他离子发生作用而形成其他物质。值得注意的是, 检测出的物质KCu3S2中存在Cu+和S2-, 这正是CH4和Na2SO4, CuO反应的产物, 说明CH4和Na2SO4, CuO发生了氧化还原反应。由色谱分析结果在产物气体中检测到CO和H2这一事实表明, 反应可能不是单纯地按着反应 (1) , (2) 描述的简单过程进行;有可能是分步进行的, 这是尚待研究的重点。待甲烷与Na2SO4, CuO反应完全后, 再向熔池中通入空气, 反应的气体产物分析结果见表2所示, 反应完全后的熔盐体系XRD分析图谱与图3 (a) 非常接近, 说明这个无烟燃烧体系的燃料燃烧过程和氧化剂生成过程可以交替连续进行。
《5 结论》
5 结论
熔融盐循环热载体无烟燃烧技术在热力学上是可行的, 对Li2CO3+K2CO3+Na2SO4为熔融盐热载体, CuO为催化剂的无烟燃烧体系进行的试验研究表明, 在燃料燃烧过程能得到纯度为77.0%~95.1%的CO2, 在氧化剂生成过程能得到纯度为91.9%~99.3%的N2, 在实现了由化学能转变成热能的同时, 并得到了较高纯度的CO2和N2, 高纯度的CO2可以方便地捕集和封存, 有利于控制化石燃料燃烧过程的温室气体排放。














 京公网安备 11010502051620号
京公网安备 11010502051620号




