《1. 引言》
1. 引言
水体中的有机微污染物(OMP),如杀虫剂、药物、内分泌干扰物(EDC)以及激素等,由于对所接触的有机体存在长期毒性刺激而对自然生态系统和生命体具有严重的负面影响[1–4]。例如,进入人体的EDC能够通过模拟天然激素的生物活性并占据激素受体而破坏人类的中枢神经系统和内分泌系统,从而干扰天然激素的传输和代谢过程,进一步危害人类以及其他生物的健康 [5–8]。因此,有效移除水中有机微污染物对保护环境和人类健康具有重要意义。
目前,移除水中OMP的方法,根据作用机理主要分为基于化学反应[9–12]、截留[13–16]以及吸附[5,17,18] 等方法。其中,化学反应,如光催化降解[19–22]通过辐射给光催化剂提供能量,从而产生电子-空穴对引发氧化还原反应,将OMP转化为无毒的无机小分子。该方法反应条件温和,氧化能力强。但是,该反应受限于 OMP的化学结构,而且需要活化催化剂。基于分子截留机理,反渗透膜和纳滤膜[13–16]等在移除水中OMP 时具有较高的截留率,但是该方法在一定程度上因操作压力高以及渗透率低等而受限[23]。特别地,基于吸附机理的移除方法,由于操作过程简单,而被广泛用于水中OMP的处理。该方法主要基于吸附剂对水中OMP 的物理或化学吸附作用而实现OMP的移除。通过在基材膜上混合[24]或接枝[25,26]功能材料而构建的吸附分离亲和膜,能够基于功能基团的特异识别作用实现对 OMP的有效捕捉。其中,基于分子识别的吸附分离功能材料,如基于环糊精(CD)及其衍生物开发的功能材料(由于环糊精分子具有外缘亲水、内腔疏水的大环空腔结构),能够作为主体分子,通过超分子作用与客体分子形成具有一定稳定性的主-客体络合物,从而实现对水中OMP的有效捕捉,使其在OMP移除领域表现出优异的性能[27–29]。基于主-客体识别络合作用,多孔CD基聚合物能够有效实现水中OMP的快速移除[30]。通过设计调控功能材料中孔的结构和性能,增大吸附位点,可以有效提高OMP的分离移除效率,但是聚合物在吸附移除OMP后,需要进一步利用膜过滤装置将其从连续相中分离。使用膜过滤工艺虽然能够提高水通量,但是该技术需要配备膜处理系统,同时面临耗时、复杂的洗膜过程,难以实现OMP的简捷移除。此外,高硅沸石[31]和碳材料[32–34],如活性炭[33]、生物碳 [32]以及介孔碳[34]等,由于具有较大的比表面积以及独特的表面特性,在用于水中OMP的移除时,也能基于吸附机理实现对水中OMP的有效移除。但是,这些方法对OMP的移除是非特异性的,且在吸附剂再生时伴有吸附剂性能显著下降的问题。因此,简捷有效移除水中OMP仍然存在挑战。
本研究中,基于超分子主-客体识别络合原理,提出了一种利用封装具有分子识别特性纳米凝胶的功能胶囊简捷有效移除水中OMP的新方法。该功能胶囊由具有半透膜特性的海藻酸钙(Ca-Alg)凝胶囊膜和具有分子识别性能的聚[N-异丙基丙烯酰胺-共聚-丙烯酸-接枝-单(6-乙二胺基-6-去氧)-β-环糊精](PNCD)纳米凝胶组成[图1(a)],是利用共挤出微流体技术构建的 [35–37]。具有分子识别特性的PNCD纳米凝胶是通过在由沉淀聚合法合成的聚(N-异丙基丙烯酰胺-共聚-丙烯酸)(PNA)纳米凝胶上接枝功能性组分单(6-乙二胺基-6-去氧)-β-环糊精而合成的。其中,具有半透膜特性的超薄Ca-Alg凝胶囊膜可以使OMP和水分子经渗透扩散跨膜传输进入囊的内部,而截留封装的PNCD纳米凝胶和高分子聚合物。双酚A(BPA)是一种可以从塑料瓶中释放的EDC [35],由于其具有毒性以及在水中分布较广而被选作OMP模型。将功能胶囊置于含有 BPA的水溶液中[图1(b)],该胶囊能够基于其封装的PNCD纳米凝胶上的功能性基团CD对BPA的识别络合作用实现BPA的等温吸附[图1(a-I)、(b-I)]。CD基团与BPA之间由于超分子疏水作用而形成了稳定的主-客体络合物CD/BPA [图1(a-III)、(b-III)],该胶囊封装的PNCD展示出BPA诱导的络合[图1(a-II)、(b-II)]。基于该络合作用,胶囊可以将BPA捕捉并封装在其内部。由于功能胶囊具有毫米尺度,基于滤网即可便捷地将胶囊从连续相BPA溶液中分离出来,从而实现水中 OMP的简捷有效移除。另外,由于所制备的PNCD纳米凝胶具有温敏性,因此进一步通过高温解吸的方法即可实现胶囊的循环再生利用。本研究提出的方法为简捷有效移除水中OMP提供了一种新的策略。
《图1》
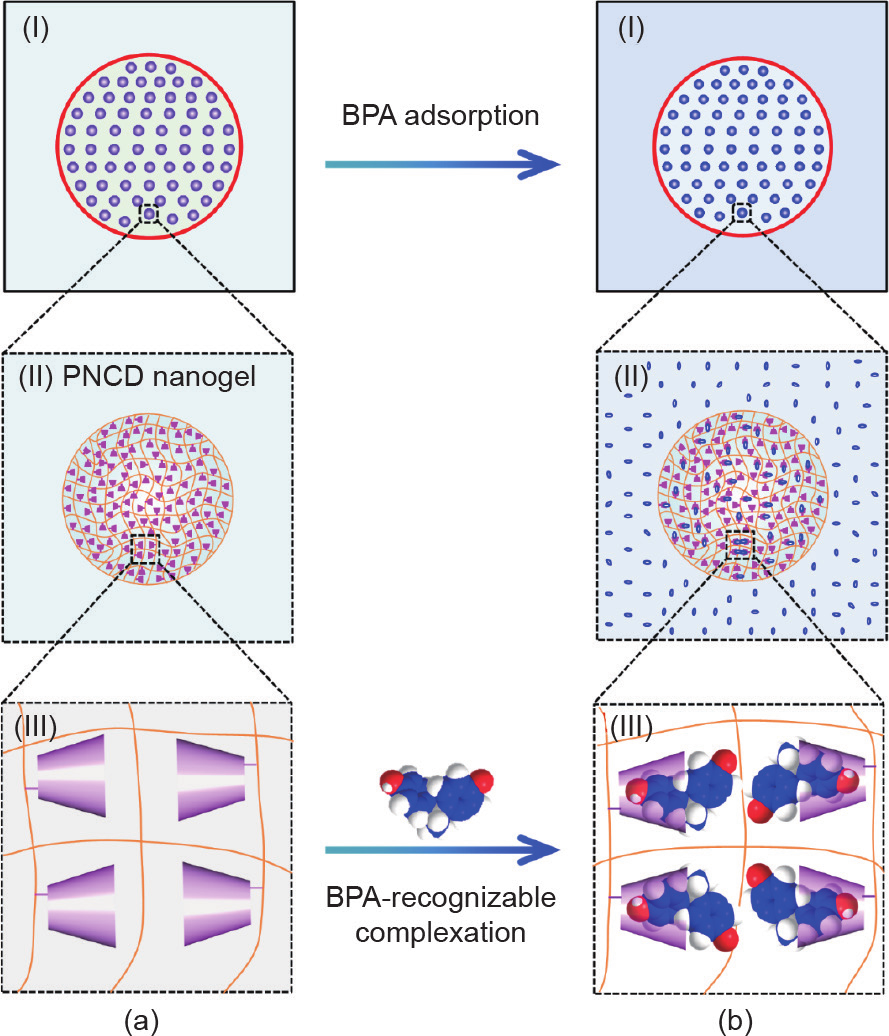
图1. 封装PNCD纳米凝胶的Ca-Alg胶囊简捷移除水中OMP的机理示意图。(a)胶囊由半透膜(I)和封装具有识别BPA特性的CD基团(III)的PNCD纳米凝胶(II)组成;(b)将胶囊添加至含有BPA的溶液中,胶囊封装的PNCD纳米凝胶中的CD基团作为主体分子,基于超分子作用以空腔识别络合客体分子BPA(a-II、b-II),形成超分子主-客体络合物CD/BPA(a-III、b-III),从而实现BPA的简捷移除。
《2. 实验部分》
2. 实验部分
《2.1. 试剂》
2.1. 试剂
本研究所用化学试剂,包括过硫酸铵(APS)、N,N′- 亚甲基双丙烯酰胺(MBA)、十二烷基硫酸钠(SDS)、丙烯酸(AAc)、海藻酸钠(Na-Alg)、羧甲基纤维素钠(CMC)以及硝酸钙[Ca(NO3)2]均采自成都市科隆化学品有限公司(中国)。单-(6-乙二胺基-6-去氧)-β-环糊精购自山东滨州智源生物科技有限公司(中国)。所用 N-异丙基丙烯酰胺(NIPAM,98%,日本东京化学工业)是经环己烷/丙酮(50/50, V/V)混合物重结晶所得。1-(3- 二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDC)购自 Sigma-Aldrich(USA)。所涉及的其他化学试剂均为分析纯级。所用去离子水(18.2 MΩ, 25 ℃)取自Milli-Q Plus水纯化系统(Millipore, USA)。
《2.2. 分子识别 PNCD 纳米凝胶的合成及表征》
2.2. 分子识别 PNCD 纳米凝胶的合成及表征
具有分子识别响应特性的PNCD纳米凝胶是通过在由沉淀共聚合成的PNA纳米凝胶网络上接枝CD基团得到的[36]。简而言之,以去离子水作溶剂,将单体AAc (0.4324 g)和NIPAM(2.7158 g)、引发剂APS(0.0685 g)、交联剂MBA(0.1203 g)以及表面活性剂SDS(0.0091 g)添加至盛有300 mL去离子水的烧瓶中,通氮气30 min 以除去水中的溶解氧,然后在70 ℃和氮气氛围的条件下密封反应4 h。待反应结束后,将其置于冰水浴中冷却15 min,然后过滤,将滤液用纯水透析以得到纯化的 PNA纳米凝胶。最后,以EDC作催化剂,在6 ℃条件下缩合反应16 h,将CD接枝在PNA纳米凝胶聚合物骨架上,制备得到PNCD纳米凝胶[见附录A中的图S1(a)、(b)]。
为了证明PNCD纳米凝胶的成功合成,利用傅里叶变换红外光谱仪(FT-IR; NICOLET iS50; Thermo Scientific, USA)对CD、PNA纳米凝胶以及PNCD纳米凝胶进行化学成分表征。在室温下将PNA和PNCD纳米凝胶干燥后喷金,利用场发射扫描电子显微镜(FESEM; JSM-7500F; JEOL, Japan)对其进行形貌表征。
为了证明PNCD纳米凝胶能够识别络合BPA,利用动态光散射(DLS; Zetasizer Nano ZEN3690; Malvern Panalytical Ltd., UK)测试高度稀释的PNCD分散液分别在纯水和0.25 mmol·L‒1 BPA溶液中的水力直径随温度的变化。测试温度范围为20 ~ 65 ℃,每隔2 ℃取一个数据点,每个温度下平衡180 s,并连续测三次。
《2.3. 构建封装 PNCD 纳米凝胶的 Ca-Alg 功能胶囊》
2.3. 构建封装 PNCD 纳米凝胶的 Ca-Alg 功能胶囊
以水包水(W/W)液滴作模板,利用共挤出微流体毛细管装置构建封装PNCD纳米凝胶的Ca-Alg功能胶囊 [37–39] [见附录A中的图S1(c)、(d)]。该技术可以实现对内外相流体的精准调控,从而精确控制液滴模板的尺寸,确保所构建的功能胶囊膜具有较好的单分散性。将方形管嵌入内径约为2.0 mm的圆管中形成共轴几何结构并将其固定于载玻片上,构建共挤出微流体装置。方形管的内外边长分别为1.0 mm和1.4 mm。利用恒流注射泵分别向方管和圆管中通入内外相流体,以在装置出口端形成W/W液滴[见附录A中的图S1(c)]。内外相流体的体积流率分别为40 mL·h–1和10 mL·h–1。内相流体为含有0.75%(m/V)CMC的PNCD纳米凝胶分散液,外相流体为含有1%(m/V)SDS的Na-Alg(2%, m/V)溶液。其中,CMC的加入是为了增大内相流体的黏度,而SDS作为乳化剂降低内外相流体间的界面张力,以形成稳定的W/W液滴[40]。在装置出口端形成W/W液滴后,立即将其滴入Ca(NO3)2(15%, m/ V)溶液中使囊壁凝胶化,构建得到封装PNCD纳米凝胶的Ca-Alg凝胶囊膜[见附录A中的图S1(d)]。通过调控内外相流体的体积流率比以控制Ca-Alg胶囊的壁厚。当外相流体的体积流率恒定时,Ca-Alg胶囊的壁厚在一定范围内随内相流体体积流率的增大而减小。反之,当内相流体体积流率恒定时,胶囊的壁厚随外相流体体积流率的增大而增大。胶囊的壁厚会影响物质的跨膜渗透效率,对于BPA的跨膜传输而言,囊壁越薄的胶囊具有更低的跨膜渗透阻力。为了探究CaAlg胶囊所封装的PNCD纳米凝胶的含量对胶囊吸附 OMP性能的影响规律,研究通过控制PNCD纳米凝胶在内相流体中的浓度([PNCD],m/V,分别为0、5 mg·mL−1、10 mg·mL−1、l5 mg·mL−1、20 mg·mL−1以及30 mg·mL−1),构建了具有不同[PNCD]的Ca-Alg胶囊。利用纯水洗涤所制备的胶囊以去除游离钙,然后将其存储于纯水中备用。采用数码相机拍摄胶囊的光学照片以观察其形貌,并通过测量其直径计算变异系数(CV)以评估胶囊的单分散性[37,38]。
《2.4. 胶囊移除水中 BPA 的最佳组成》
2.4. 胶囊移除水中 BPA 的最佳组成
为了确定胶囊移除水中BPA的最佳组成,我们研究了[PNCD]对胶囊吸附性能的影响规律。具体方法为:分别取数量为5颗、10颗、20颗、30颗和40颗的封装0、 5 mg·mL−1、10 mg·mL−1、l5 mg·mL−1、20 mg·mL−1以及 30 mg·mL−1 PNCD的功能胶囊于2 mL 0.5 mmol·mL−1的 BPA溶液中,将温度控制在25 ℃,按时取样,利用微量紫外仪(NanoDrop One, Thermo Scientific, USA)测定取样BPA溶液在最大吸收波长λmax = 276 nm处的紫外吸光度,然后基于标准曲线计算BPA的浓度([BPA]),研究胶囊中[PNCD]对胶囊吸附性能的影响。利用下式 [30]计算胶囊对BPA的吸附效率R:
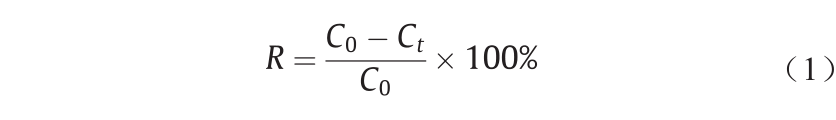
式中,C0和Ct分别表示BPA在原液中的初始浓度和在时间t (单位为min)时对应的浓度,单位为mmol·L−1。
胶囊吸附BPA的质量Qt的计算公式[30]如下:

式中,Qt表示胶囊在时间t时吸附的BPA的总质量(mg);qt 表示在时间t时胶囊内单位质量PNCD纳米凝胶吸附的BPA 的质量(mg·g−1);M为BPA的摩尔质量(g·mol−1);V为BPA 溶液的体积(L);m表示吸附实验使用的PNCD纳米凝胶的总质量(g),可以由下式计算得到:
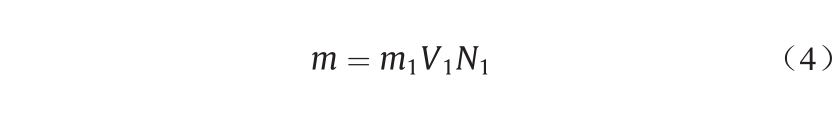
式中,m1表示胶囊内封装的PNCD的浓度(mg·mL−1);V1表示每颗胶囊的体积(L);N1表示吸附实验时所使用的胶囊颗数。
为了研究胶囊的吸附动力学,利用拟二级吸附动力学模型来描述胶囊对BPA的吸附速率,该模型如下式 [41,42]所示:

式中,qe表示平衡时胶囊内单位质量PNCD纳米凝胶吸附的BPA的质量(mg·g−1);Kobs为表观二级速率常数(g·mg−1·min−1)。
《2.5. 胶囊对 BPA 的吸附热力学》
2.5. 胶囊对 BPA 的吸附热力学
为了研究胶囊移除BPA的等温吸附热力学,我们研究了[BPA]对胶囊的吸附性能的影响规律。具体操作方式为:在[BPA]分别为0.025 mmol·L−1、0.05 mmol·L−1、 0.1 mmol·L−1、0.3 mmol·L−1、0.5 mmol·L−1、 0.7 mmol·L−1和0.9 mmol·L−1的2 mL BPA溶液中加入 20 颗封装15 mg·mL−1 PNCD纳米凝胶的胶囊,控制温度为25 ℃,按时取样测定外部溶液中的[BPA]。分别利用式(1)和式(3)计算胶囊对BPA的移除效率R和吸附质量qt ,并利用Langmuir、Freundlich以及Redlich-Peterson等温吸附模型定量分析胶囊对BPA的热力学吸附机理。其中,利用1/qe对1/Ce作图可以拟合得到Langmuir 等温吸附模型,如下式[25,30]所示:
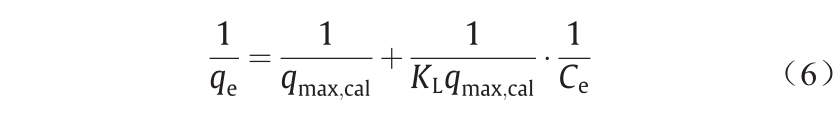
式中,qmax,cal表示胶囊理论上的最大平衡吸附容量(mg·g−1); Ce表示吸附达平衡后的[BPA](mmol·L−1);KL为平衡常数。
利用lnqe对lnCe作图可拟合得到Freundlich等温吸附模型,如下式[25]所示:
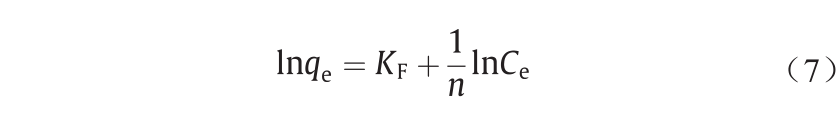
式中,KF和n为Freundlich常数。
利用Ce/qe对Ce作图可拟合得到Redlich-Peterson等温吸附模型,如下式[43]所示:

式中,A和B为Redlich-Peterson常数;β为0~1之间的系数。
《2.6. 胶囊的热力学行为及再生实验研究》
2.6. 胶囊的热力学行为及再生实验研究
为了进一步研究功能胶囊对BPA的吸附热力学行为,我们研究了温度对胶囊吸附性能的影响。基于温度对PNCD纳米凝胶识别响应BPA性能的影响研究结果发现,当温度从20 ℃增加至32 ℃时,PNCD的水力直径在0.25 mmol·L−1的BPA溶液中几乎保持不变,表明在该温度范围内PNCD对BPA的识别不受温度的影响;在进一步将温度从32 ℃升高至60 ℃的过程中,由于聚(N-异丙基丙烯酰胺)(PNIPAM)骨架的存在,PNCD的水力直径呈现明显的热响应体积收缩行为;而进一步将温度升高至60 ℃以上后,其又几乎保持不变。因此,选择25 ℃、50 ℃和60 ℃作为研究胶囊吸附热力学行为的温度点,分别在上述三个温度点下进行胶囊对BPA的吸附实验。具体操作方式为:控制溶液温度分别为25℃、 50 ℃和60 ℃,在浓度为0.1 mmol·L−1、0.3 mmol·L−1、 0.5 mmol·L−1、0.7 mmol·L−1和0.9 mmol·L−1的2 mL BPA溶液中分别加入20颗封装15 mg·mL−1的PNCD纳米凝胶的胶囊,对其进行吸附。测试胶囊外部溶液中[BPA]随时间的变化关系,直至达到吸附平衡。利用热力学参数 Gibbs自由能变化(△G)、焓变(△H)以及熵变(△S)来评估该吸附过程的热力学行为,这些热力学参数由下面的Van’t Hoff方程[5,17,44,45]计算得到:

式中,Rg为气体常数(8.314 J·mol−1·K−1);T为BPA溶液的温度(K);由lnKL对T ‒1拟合的斜率计算ΔH。
为了考察胶囊的再生特性,对胶囊对BPA的吸附-解吸性能进行研究。在25 ℃下,将20颗封装15 mg·mL−1 PNCD纳米凝胶的胶囊置于2 mL 0.5 mmol·L−1的BPA溶液中对其进行吸附,测试[BPA],直至达到吸附平衡。待其达到吸附平衡后,在50 ℃下利用2 mL纯水置换BPA溶液,反复洗涤,直至加入纯水后的溶液中[BPA]不再发生变化。再次将上述解吸后的胶囊置于温度为25 ℃的2 mL 0.5 mmol·L−1的BPA溶液中对其进行吸附,然后在50 ℃下进行解吸,反复若干次。当胶囊完成解吸后,利用筛网过滤即可将胶囊从连续相BPA溶液中分离出来。胶囊的解吸效率Rd计算公式如下所示:
 v
v
式中,Qd表示达到解吸平衡时胶囊解吸的BPA的总质量(mg);Qe表示达到吸附平衡时胶囊吸附BPA的总质量(mg)。
《3. 结果与讨论》
3. 结果与讨论
《3.1. PNCD 纳米凝胶的化学成分及形貌表征》
3.1. PNCD 纳米凝胶的化学成分及形貌表征
利用FT-IR分别对CD、PNA纳米凝胶和PNCD纳米凝胶进行化学成分表征,结果如附录A中的图S2所示。由图S2可知:波数1388 cm−1和1368 cm−1处为NIPAM 中的异丙基吸收峰,其在PNA和PNCD中均存在,表明PNA和PNCD中均存在PNIPAM骨架;同时,波数 1034 cm−1为CD的特征吸收峰,在CD和PNCD中均存在,而在PNA中没有;另外,在波数1716 cm−1处出现的PNA上的羧基振动吸收峰在PNCD中几乎不存在,说明PNA中的羧酸基团基本全部与CD中的氨基反应生成了PNCD。上述结果表明实验成功合成了PNCD,并且,由PNA(见附录A中的图S3)和PNCD [图2(a)]在干态下的SEM图可以看出,所制备的PNA和PNCD纳米凝胶具有良好的球形度。
《图2》
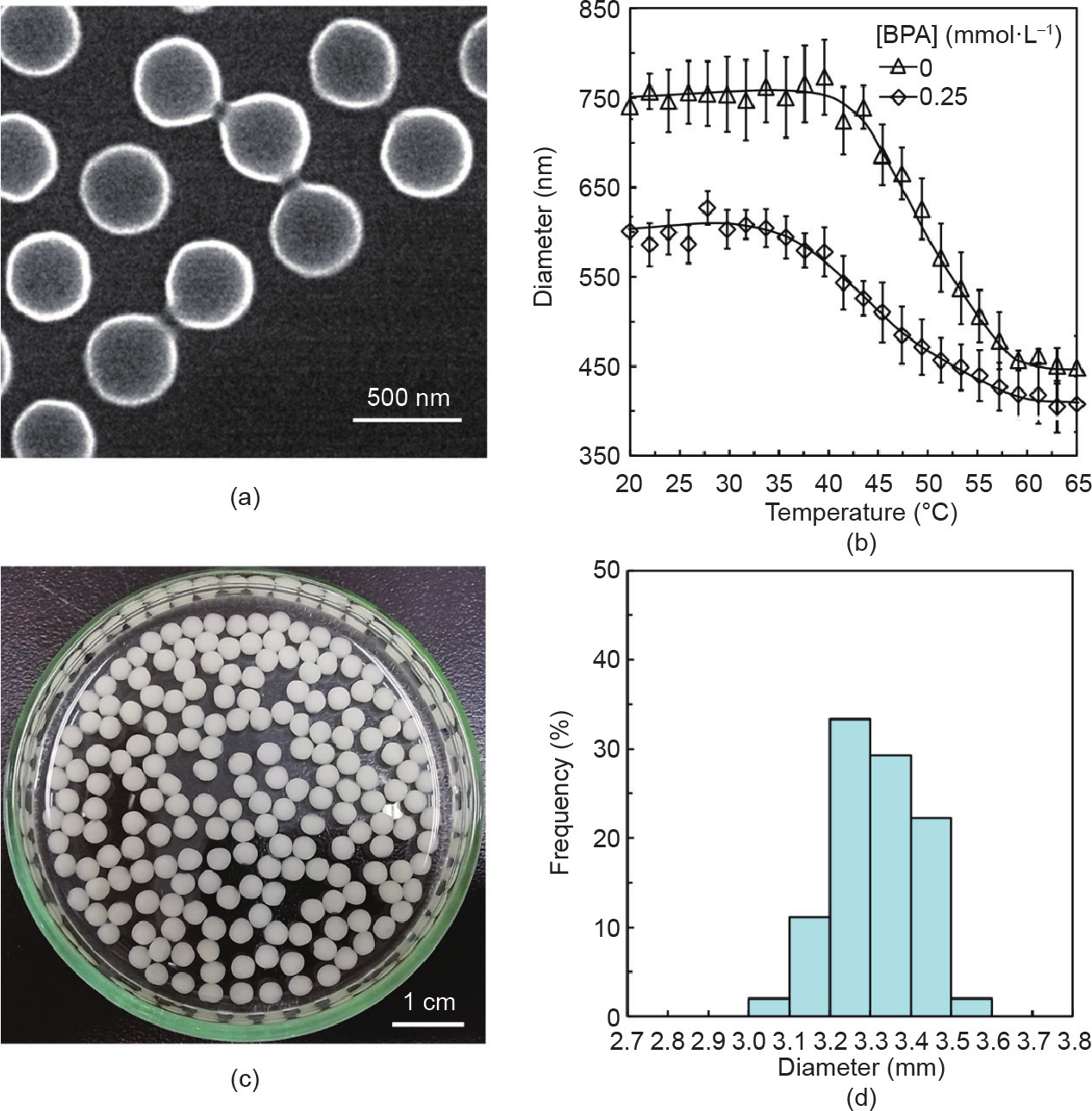
图2.(a)PNCD纳米凝胶在干态下的SEM图;(b)PNCD纳米凝胶分散液分别在纯水和0.25 mmol·L–1 BPA溶液中的水力直径随温度的变化关系;封装15 mg·mL–1 PNCD纳米凝胶的功能胶囊的光学照片(c)及其尺寸分布图(d)。
《3.2. PNCD 纳米凝胶的分子识别性能》
3.2. PNCD 纳米凝胶的分子识别性能
PNCD纳米凝胶的温度和分子识别响应特性研究结果如图2(b)所示。由图2(b)可知:在同一温度下, PNCD纳米凝胶在0.25 mmol·L–1 BPA溶液中的水力直径总是小于其在纯水中的水力直径。其原因主要是PNCD 中的CD基团与BPA分子之间的超分子主-客体络合作用诱导凝胶网络收缩[图1(a-III)、(b-III)] [29,46]。当 PNCD与BPA络合时,非极性的客体分子BPA部分进入 CD的疏水空腔,基于尺寸效应以及超分子作用与之形成稳定的主-客体络合物CD/BPA。该络合作用使得BPA 中的另一个疏水苯基暴露在CD腔体之外,从而增大了 PNCD凝胶网络的疏水性,导致PNCD捕捉BPA后体积减小。同时,由图2(b)可知:在20~65 ℃范围内,随着温度的升高,由于PNIPAM骨架的存在,PNCD纳米凝胶在纯水和0.25 mmol·L–1 BPA溶液中表现出热致体积收缩行为[47,48]。上述结果表明,所制备的PNCD纳米凝胶能够识别响应BPA。
《3.3. 封装 PNCD 的功能胶囊的形貌表征》
3.3. 封装 PNCD 的功能胶囊的形貌表征
Ca-Alg胶囊的囊膜厚度随着内外相流体体积流率比Qi/Qo的增大而减小[49]。较薄的囊膜厚度使得其对 BPA的跨膜传输具有较小的渗透阻力。为了获得一个相对较合适的囊膜厚度,研究将Qi和Qo分别固定为 40 mL·h−1和10 mL·h−1。其中,较合适的囊膜厚度,首先要求胶囊具有较薄的壁厚使得BPA具有较低的跨膜渗透阻力,而且要求在操作过程中胶囊壁不会破裂。以封装15 mg·mL−1 PNCD纳米凝胶为例,由其光学图片[图 2(c)]和尺寸分布[图2(d)]可知,该胶囊的形貌具有较好的球形度,且尺寸分布较窄,具有较好的尺寸均一性。计算得到胶囊的平均直径约为3.32 mm,CV值为 3.03%。这种较好的单分散性可以提高胶囊吸附性能的可重复性。
《3.4. 功能胶囊对 BPA 的吸附特性》
3.4. 功能胶囊对 BPA 的吸附特性
为了确定胶囊用于BPA吸附的最佳组成,研究 [PNCD]和胶囊颗数对其吸附性能的影响。首先,为了证明胶囊对BPA的吸附主要由PNCD主导,在25 ℃下研究了不含PNCD纳米凝胶的Ca-Alg胶囊对0.5 mmol·L–1 BPA溶液的吸附性能,结果如图3(a)、(b)所示。由图3(a)、(b)可以看出,随着时间的增加,不同颗数的胶囊吸附BPA的总质量Qt [图3(a)]和移除率R [图 3(b)]均呈现先增大后减小最后趋于稳定的趋势,且在同一时刻,胶囊对BPA的吸附总质量Qt和移除率 R均随胶囊的颗数增大而增大。胶囊颗数在5~40颗时,对应的BPA吸附总质量Qt和移除率R的范围分别为 0.005~0.047 mg和2.5%~20%。上述结果表明,未封装 PNCD的胶囊对BPA存在微弱的吸附作用。其主要原因是胶囊的Ca-Alg凝胶网络对BPA存在弱物理吸附作用,当囊壁内外存在的BPA浓度差驱动BPA向胶囊内腔室扩散传输时,BPA首先与胶囊的Ca-Alg凝胶网络接触,基于凝胶网络对BPA的氢键和范德瓦耳斯力作用,凝胶网络能够部分吸附BPA。同时,胶囊在吸附BPA的过程中,随着时间的增加,对应的Qt和R呈现先增大后减小的原因是胶囊吸附BPA后,由于弱的物理作用不能将BPA稳定在胶囊内部(BPA在凝胶囊膜半透膜中可以自由跨膜传输),使得其解吸后从囊内或囊壁反向渗透跨膜传输。
相比于空白的Ca-Alg胶囊,封装PNCD纳米凝胶的胶囊能够显著增强其对BPA的吸附性能。以封装5 mg·mL−1 PNCD的胶囊为例,当其颗数为5~40颗时,对应的Qt [图3(c)]和R [图3(d)]的范围分别为 0.041~0.171 mg和17.9%~74.8 %;相对于未封装PNCD 的空白胶囊,其吸附率提高了15.4%~54.8 %,是空白胶囊的3.74~7.12倍。PNCD的添加增强了胶囊对BPA的吸附性能,其主要原因是PNCD提供了更多有效的吸附位点,当BPA跨膜传输进入胶囊的内腔室后,其中PNCD 上的CD基团作为主体分子,基于超分子作用以疏水空腔识别络合客体分子BPA,这种化学吸附作用进一步增强了BPA与PNCD的结合力,从而形成稳定的主-客体络合物CD/BPA,并且在达到吸附平衡前进一步吸附 BPA时不会产生BPA的解吸。
另外,对于qt而言,由于其描述的是单位质量 PNCD吸附的BPA的质量,从图3(e)可以看出,在同一时刻,随着胶囊颗数的增多,封装不同[PNCD]的胶囊对BPA的qt均呈现减小的趋势。表明单位质量PNCD吸附的BPA的质量随着胶囊颗数的增大而减小。其原因是当CD相对于BPA的量增大后,一个CD基团能够均匀捕获一个BPA分子的概率下降。上述结果表明,虽然在一定浓度范围内,PNCD提供的吸附位点越多,就越可以提高其对吸附质的吸附效率,但实际发挥吸附作用的有效位点相对减少。同时,利用准二级吸附动力学模型对胶囊吸附BPA的实验数据进行拟合,结果如图3(f)所示。由图3(f)可知,胶囊对BPA的吸附动力学符合准二级吸附动力学,其中PNCD提供的功能基团CD作为吸附位点与BPA络合的化学吸附过程为该吸附过程的主要速率限制步骤。上述结果表明,在胶囊吸附BPA 时,其内部封装的PNCD纳米凝胶中的CD基团识别络合BPA形成超分子主-客体络合物的化学过程对其吸附起主导作用。
《图3》
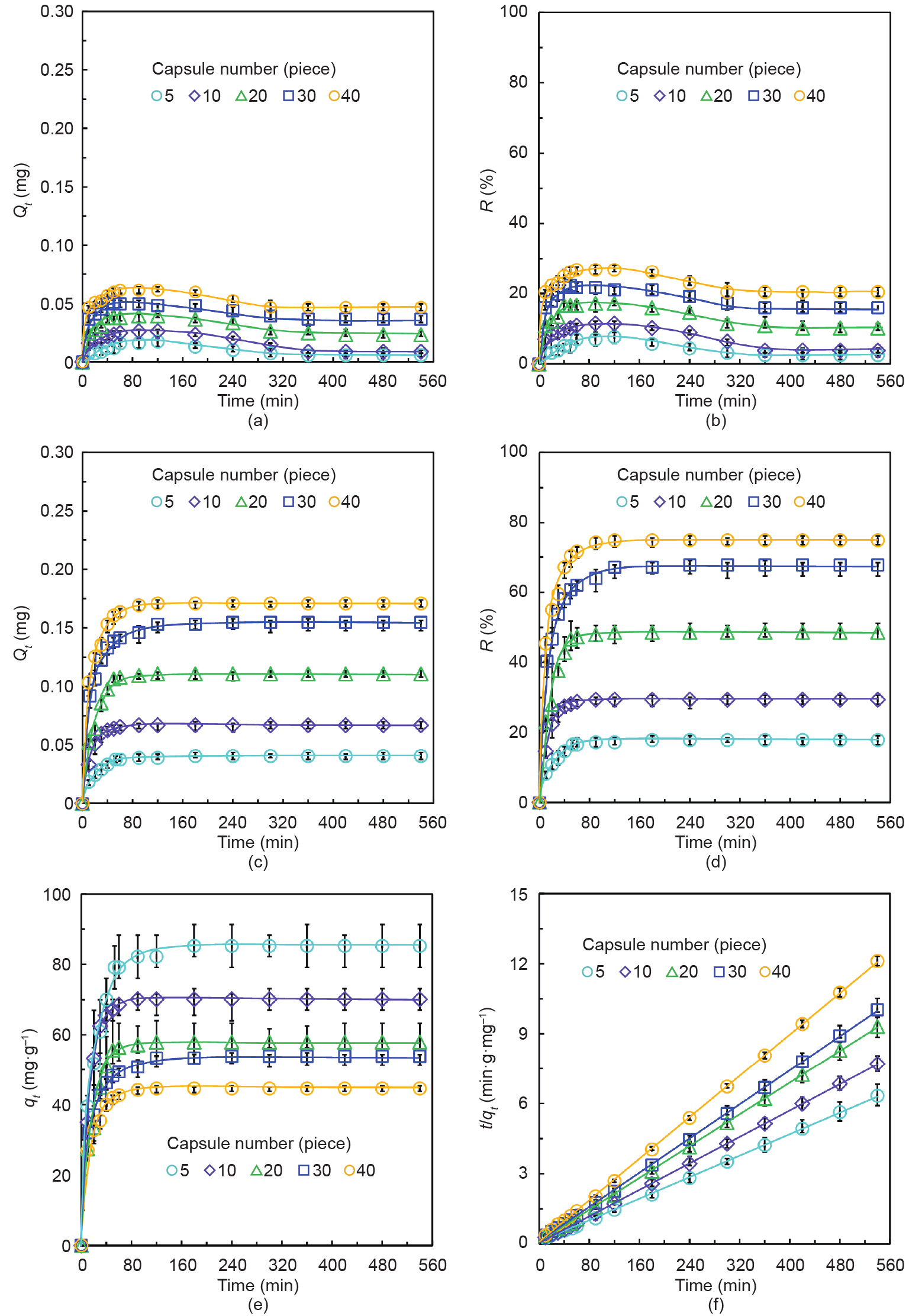
图3. 封装不同[PNCD]纳米凝胶的胶囊在25 ℃时对0.5 mmol·L−1 BPA的吸附特性。不含PNCD纳米凝胶的胶囊在不同颗数下吸附BPA的Qt (a)和 R(b)随时间的变化关系;封装5 mg·mL–1 PNCD纳米凝胶的胶囊在不同颗数下吸附BPA的Qt (c)、R(d)和qt (e)随时间的变化关系,以及对应的准二级动力学插值(f)。
同时,对于分别封装10 mg·mL–1(见附录A中的图 S4)、15 mg·mL–1(见附录A中的图S5)、20 mg·mL–1(见附录A中的图S6)以及30 mg·mL–1(见附录A中的图 S7)PNCD纳米凝胶的胶囊,其对应的Qt [见附录A中的图S4(a)~S7(a)]、R [见附录A中的图S4(b)~S7(b)]、以及qt [见附录A中的图S4(c)~S7(c)]随时间的变化规律均相似,且其对BPA的吸附动力学同样满足拟二级模型[见附录A中的图S4(d)~S7(d)]。
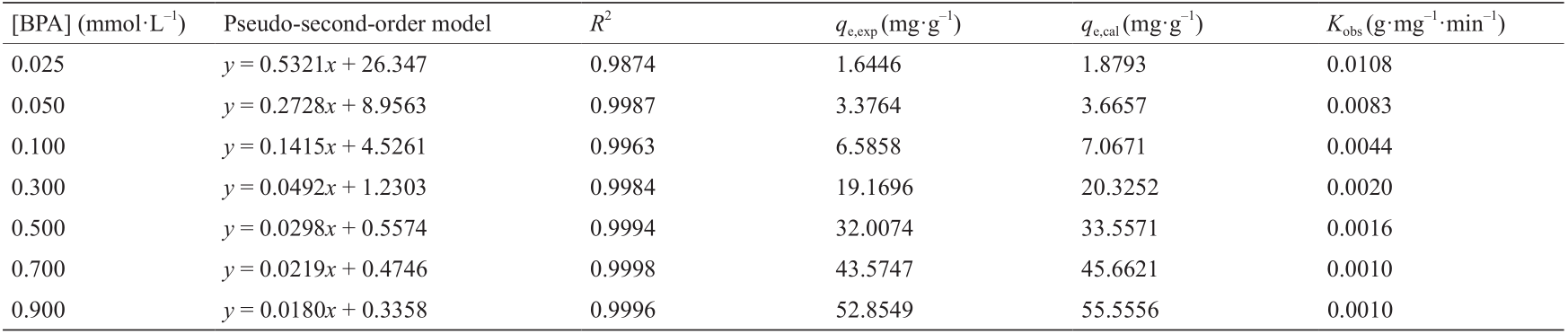
对于所封装的[PNCD]在0~30 mg·mL–1的胶囊(图 4),分别用5颗和10颗胶囊对BPA进行吸附,其对应的总吸附质量Qe [图4(a)]以及移除率R [图4(c)]均随 [PNCD]增大而增大;而当用20颗、30颗或40颗胶囊对 BPA进行吸附时,其对应的Qe以及R均随[PNCD]增大呈现先增大后趋于不变的趋势,且对应的转折点均出现在[PNCD] = 15 mg·mL–1处。由于20颗封装15 mg·mL–1 PNCD的胶囊对于2 mL 0.5 mmol·L–1 BPA的吸附率能够达到80%,因此实验选择封装15 mg·mL–1 PNCD的胶囊作进一步研究。对于封装不同[PNCD]的胶囊,其吸附BPA的qe随[PNCD]的增大而减小[图4(b)],表明[PNCD]越大,单位质量PNCD吸附的BPA的质量越小。附录A中的表S1展示了封装不同[PNCD]的胶囊对 0.5 mmol·L–1 BPA的吸附拟二级动力学插值结果,包括拟二级动力学模型、Kobs(g·mg–1·min–1)、实验中的平衡吸附质量qe,exp(mg·g–1)以及理论平衡吸附质量qe,cal(mg·g–1)),结果显示qe,exp与qe,cal的值几乎相同,表明实验所制备的胶囊对BPA的吸附动力学符合拟二级动力学模型。
《图4》
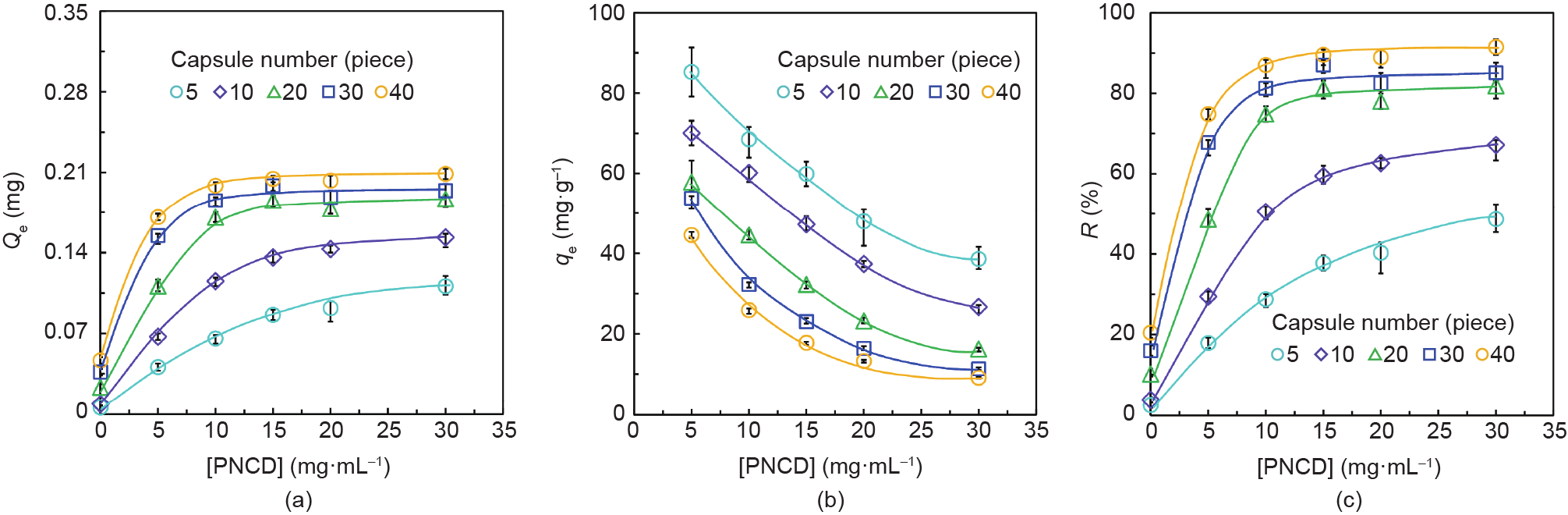
图4. 在25 ℃时,[PNCD]对胶囊吸附0.5 mmol·L–1 BPA的性能的影响。不同颗数的胶囊对BPA的Qe (a)、qe (b)以及R(c)随[PNCD]的变化关系。
《3.5. 功能胶囊对 BPA 的吸附动力学和热力学》
3.5. 功能胶囊对 BPA 的吸附动力学和热力学
为了研究功能胶囊对BPA的吸附动力学和热力学,进一步对封装15 mg·mL−1 PNCD的胶囊对不同[BPA]的吸附特性进行研究,结果如图5所示。由图5(a)、(b)可知,对于[BPA]为0.025~0.9 mmol·L−1的BPA溶液,随着时间的增大,胶囊吸附BPA的Qt [图5(a)]和qt [图5 (b)]均呈现先增大、后趋于稳定的趋势,表明经过一定时间后吸附达到了平衡;同时,对于不同[BPA],由于PNCD提供的吸附位点足够多,使得在同一时刻,Qt 和qt均随[BPA]的增大而增大,且平衡吸附质量Qe和qe 也随[BPA]的增大而增大,即对于高浓度的BPA,胶囊吸附的BPA质量以及单位质量PNCD吸附的BPA的质量也更多。另外,由图5(c)中可以看出,当[BPA]为 0.025~0.5 mmol·L−1时,胶囊对BPA的吸附率基本保持在80%以上;而当[BPA]进一步增大至0.9 mmol·L−1时,由于胶囊中PNCD提供的结合位点有限,与BPA作用后,其结合位点逐渐达到饱和,无法对高浓度的BPA 提供足够多的结合位点,使得其吸附率呈现轻微的减小。进一步利用准二级动力学模型对其吸附数据进行拟合,结果如图5(d)和表1所示。由图5(d)可知,当 [PNCD]固定时,对于不同的[BPA],胶囊吸附BPA的拟合结果曲线t/qe-t的斜率随着[BPA]的增大而减小。结合式(6)分析可知,这是由于其对应的平衡吸附质量qe 随着[BPA]的增大而增大[图5(b)]造成的。由表1可知,实验所得的qe,exp值接近于qe,cal.值,且对应的拟合相关系数R2 均接近于1,表明胶囊对不同[BPA]的吸附动力学同样符合准二级吸附动力学,且功能基团CD与BPA络合的化学吸附过程为该吸附的主要速率限制步骤。值得一提的是,从表1可以看出,[BPA]越高,对应的准二级动力学模拟结果对其具有更高的相关系数,表明拟二级动力学对较高浓度的BPA的吸附结果具有更高的适用性。同时,对于不同的[BPA],其表观二级速率常数Kobs随着[BPA]的增大而减小。其原因是高浓度的BPA具有更高的推动力,传质速率更快,使得胶囊在单位时间内吸附BPA的量越多。上述结果表明,[BPA]越大,吸附速率越快,胶囊吸附BPA所需的时间更少。
《图5》
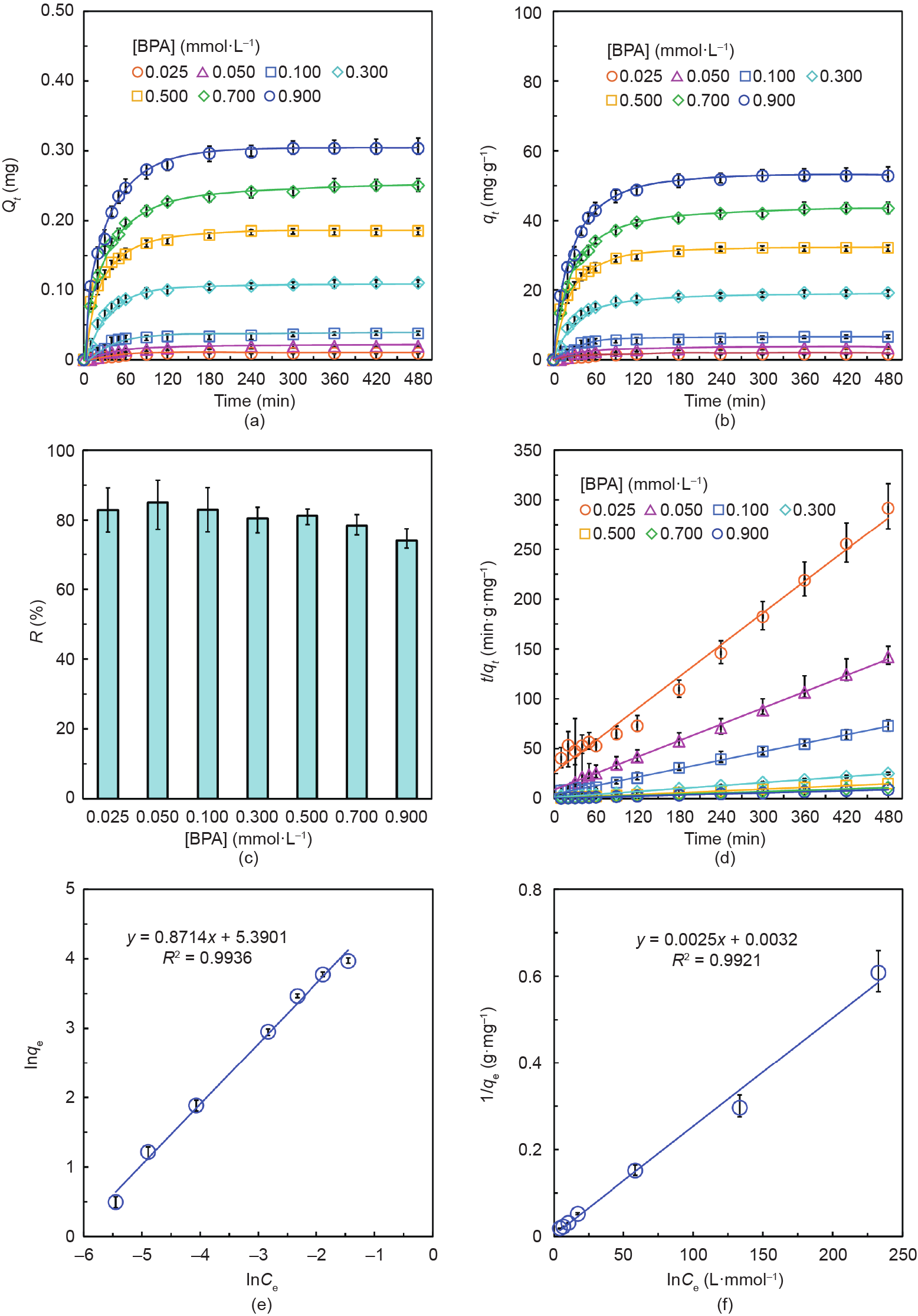
图5. 封装15 mg·mL−1 PNCD纳米凝胶的胶囊在25 ℃时对不同[BPA]的吸附性能。胶囊对不同[BPA]的Qt (a)和qt (b)随时间的变化关系;胶囊吸附不同[BPA]的平衡移除率R(c)以及准二级动力学插值(d);胶囊吸附BPA的Freundlich(e)和Langmuir(f)等温吸附热力学模型插值。
《表1》
表1 封装15 mg·mL–1 PNCD纳米凝胶的胶囊吸附不同[BPA]的拟二级插值结果
进一步利用Freundlich、Langmuir以及Redlich-Peterson等温吸附模型研究胶囊对BPA的吸附热力学,结果显示,Freundlich [图5(e)]、Langmuir [图5(f)]以及Redlich-Peterson [见附录A中的图S8]等温模型的相关系数R2 分别为0.9936、0.9921和0.9398,说明Freundlich 和Langmuir模型均具有较好的拟合度,适用于描述该胶囊对BPA的吸附行为。同时,由于Freundlich等温模型的相关系数R2 略大于Langmuir等温模型,说明Freundlich等温模型更加适用于描述该功能胶囊对BPA的吸附过程。上述结果表明,胶囊对BPA的吸附机理是在胶囊内部PNCD纳米凝胶上发生的以CD识别络合BPA的化学吸附占主导地位的多分子层吸附,该吸附过程同时伴有Ca-Alg凝胶对BPA的物理吸附,为非均相吸附过程[30,50]。并且,Freundlich等温模型的n值约等于 1.15,表明封装PNCD纳米凝胶的胶囊对BPA的吸附是有利的。
此外,为了进一步研究胶囊对BPA的吸附热力学机理,在25 ℃、50 ℃和60 ℃下研究封装15 mg·mL−1 PNCD的胶囊对0.5 mmol·L−1 BPA的吸附特性,结果如图6所示。由图6(a)、(b)可知,胶囊在不同温度下吸附BPA的热力学行为同样符合Freundlich [图6(a)]以及Langmuir [图6(b)]等温吸附模型。并且,在同一温度下,当[BPA]在0.1 ~ 0.9 mmol·L−1时,胶囊对BPA的移除率R随着[BPA]的增大呈现轻微的下降;同时,对于同一[BPA],随着温度从25 ℃升高至60 ℃,R也呈现轻微下降的趋势[图6(c)]。原因是温度升高打破了体系的热力学平衡态,使得PNCD与水分子之间的氢键作用被破坏,从而导致其从亲水溶胀状态转变为疏水收缩状态,PNCD凝胶网络的空间位阻增大;同时,温度升高导致分子布朗运动速率加快,使得PNCD中的CD功能基团与BPA之间的络合常数下降,从而造成PNCD中CD 有效络合的BPA分子的量减少,由此造成胶囊对BPA的移除率R随温度升高呈现轻微减小的状态。进一步利用 Van’t Hoff方程对实验数据进行拟合,研究其吸附行为,结果如图6(d)和表2所示。由图6(d)可知该模型的拟合相关系数R2 为0.9018,具有较好的拟合度。同时,基于式(9)和式(10)计算可得胶囊吸附BPA的过程中相关的热力学参数,其中焓变ΔH = − 5407.7 J·mol−1,熵变ΔS = 50.83 J·mol−1·K−1。由表2可知对于不同温度下的Gibb’s自由能变化ΔG < 0。上述结果表明胶囊吸附 BPA的过程为放热(ΔH < 0)的熵增过程(ΔS > 0),而这也进一步解释了BPA的R随温度升高呈现下降趋势的原因。同时,该吸附过程也是一个自发的过程(ΔG < 0)。
《图6》

图6. 封装15 mg·mL−1 PNCD纳米凝胶的胶囊对BPA的吸附热力学。胶囊在不同温度下吸附BPA的Freundlich(a)以及Langmuir(b)等温吸附热力学模型拟合曲线;胶囊在不同温度下对不同[BPA]的平衡吸附率R(c)以及Van’t Hoff拟合曲线(d)。
《表2》
表2 封装15 mg·mL–1 PNCD纳米凝胶的胶囊在25 ℃、50 ℃以及 60 ℃时吸附BPA的热力学参数

《3.6. 移除 BPA 的功能胶囊的再生特性》
3.6. 移除 BPA 的功能胶囊的再生特性
通过在高于PNCD的体积相转变温度(VPTT)条件下对吸附了BPA的胶囊进行水洗,以考察其再生性能。其具体方式为:使胶囊先在25 ℃下吸附0.5 mmol·L−1 BPA达平衡,然后用50 ℃的去离子水置换BPA溶液对其进行解吸,如此吸附-解吸循环6次,结果如图7所示。胶囊吸附-解吸的机理主要是基于其中的PNCD的温度和分子识别响应特性。如图7(a)所示,当温度低于其VPTT(如25 ℃)时,PNCD的凝胶网络处于亲水溶胀状态,CD基团与BPA络合形成稳定的主-客体络合物,从而吸附BPA;而当温度高于其VPTT(如50 ℃)时,PNCD的凝胶网络发生相变,从亲水溶胀状态转变为疏水收缩状态,使得CD基团与BPA之间的络合常数降低,络合作用减弱,导致BPA易于从CD的疏水空腔解吸[46]。解吸的BPA分子在胶囊内外浓度差的驱动下,从内核中渗透Ca-Alg凝胶网络囊膜,然后传输进入外部水溶液中,从而实现BPA的解吸。由图7(b)可知,经过6次吸附-解吸的循环操作后,该胶囊对0.5 mmol·L−1 BPA的吸附率仅展现出轻微的下降(约为4.5%)。并且,由图7(c)可以看出,该胶囊具有优异的BPA解吸性能,在6次吸附-解吸循环过程中,其解吸率Rd均能保持在 90%以上。因此,该胶囊具有优异的再生特性,可以通过高温水洗解吸实现重复使用。通常情况下,所制备的 Ca-Alg胶囊在纯水中可至少保存半年以上并仍能保持其特性;然而,由于强酸/碱环境会导致海藻酸链中的羧基质子化/去质子化,从而使得凝胶网络被破坏,胶囊容易破裂。因此,该功能胶囊更适合存储于去离子水中。
《图7》
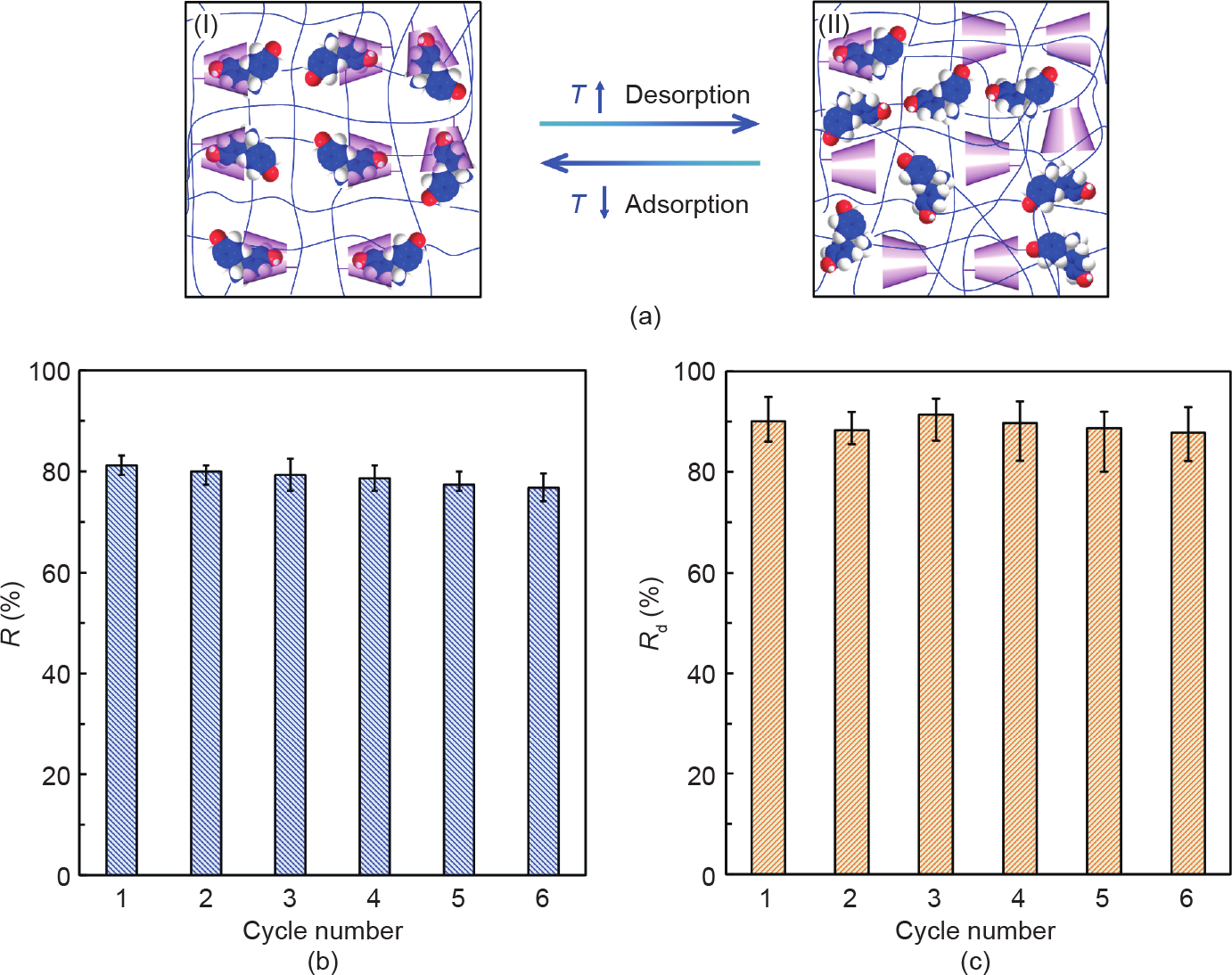
图7. 封装15 mg·mL−1 PNCD纳米凝胶的胶囊对BPA的吸附-解吸性能。(a)胶囊的低温吸附(I)和高温解吸(II)机理示意图;胶囊吸附0.5 mmol·L−1 BPA时吸附-解吸循环6次对应的平衡吸附率R(b)和解吸率Rd(c)。
《4. 结论》
4. 结论
综上,本研究提出了一种利用封装具有分子识别特性纳米凝胶的功能胶囊简捷有效移除水中OMP的新方法。该功能胶囊由半透膜和封装了具有BPA识别特性的 CD基团的PNCD纳米凝胶组成。其中,半透膜可以使 BPA和水分子自由跨膜传输进入囊的内部,而截留封装的PNCD纳米凝胶。基于主-客体识别络合作用,PNCD 纳米凝胶上的CD基团能够有效捕捉BPA分子。因此,通过将胶囊置于含有BPA的水溶液中,即可利用其实现水中OMP的简捷有效移除。并且,由于胶囊具有毫米尺度的特点,进一步利用滤网筛分即可便捷地将胶囊从溶液中分离出来。该胶囊对BPA展现出优异的移除效率,且其对应的平衡移除率随所封装[PNCD]的增大而增大,对应的吸附动力学符合拟二级动力学模型,等温吸附热力学同时满足Freundlich以及Langmuir等温吸附模型。该功能胶囊对BPA的吸附机理主要为其中的 PNCD上的CD基团与BPA络合的化学吸附,且该吸附过程是放热的熵增过程。此外,由于所制备的功能胶囊具有温敏性,进一步利用纯水在高于PNCD纳米凝胶的 VPTT的条件下反复清洗胶囊即可实现胶囊的循环再生利用。因此,本研究提出的基于分子识别纳米凝胶的功能胶囊的方法为简捷有效移除水中OMP提供了一种新的策略。
《致谢》
致谢
感谢国家自然科学基金项目(21991101)。
《Compliance with ethics guidelines》
Compliance with ethics guidelines
Wen-Ying Liu, Xiao-Jie Ju, Xing-Qun Pu, Quan-Wei Cai, Yu-Qiong Liu, Zhuang Liu, Wei Wang, Rui Xie, and Liang-Yin Chu declare that they have no conflict of interest or financial conflicts to disclose.














 京公网安备 11010502051620号
京公网安备 11010502051620号




