《1、 引言》
1、 引言
软磁材料在电磁转换应用中具有重要意义[1]。与铁氧体相比,软磁合金具有更高的饱和磁化强度和磁导率,但其高频应用受制于涡流损耗。为了解决这一难题,已有研究致力于开发金属磁粉分散于绝缘基体的软磁复合材料(SMCs)[2‒3]。获得该结构的关键在于磁粉表面的绝缘包覆,其对提高电阻率和抑制涡流损耗至关重要[4]。依据在绝缘处理过程中金属磁粉是否参与反应,可将包覆层的形成分为两种情况。一种是使用溶胶-凝胶[5‒7]、共沉淀[8]等磁粉不参与反应的方法获得Al2O3、MgO和SiO2等包覆层。此类方法制备的包覆层与磁粉的结合性相对较差,且在压制成型时易开裂,降低材料性能。另一种方法采用钝化液,如酸或具有氧化性的盐溶液,与金属磁粉元素直接反应形成包覆层[9‒10]。与溶胶-凝胶和共沉淀法相比,磁粉与氧化性溶液原位反应形成的包覆层具有更好的结合强度且有利于工业化生产。例如,通过磷酸钝化生成磷酸盐包覆层在研究和生产中应用最为广泛[11‒12]。然而,磷酸盐在温度高于600 ℃时易分解[13],限制了后续去应力退火的温度。因此,亟需发展新的绝缘包覆技术,获得具有良好热稳性,与基体紧密结合,厚度薄且均匀完整包覆的绝缘层。此外,深入理解钝化过程中的热力学和动力学机制,对于实现湿化学钝化条件的精准调控具有重要意义。
本工作基于应用广泛的FeSiAl软磁合金,其具有高磁导率、低磁致伸缩性和各向异性的特点,发明了适合现有工业生产条件的NaNO3可控钝化技术。通过精细的电镜观察以及热力学和动力学分析,揭示了包覆层在不同条件下成分组成和微观结构的演变,并明确了包覆层演变与磁性能的关联机制。
《2、 实验方法》
2、 实验方法
采用NaNO3溶液(10.0wt%~30.0wt%, 30.0 mL)作为钝化液,通过CH3COOH/CH3COONa缓冲液调控钝化液的pH为2~8(NaNO3、CH3COOH及CH3COONa均购买自国药集团有限公司)。将30wt%的50 µm粒度和70wt%的75 µm粒度的Fe-9.6wt%Si-5.4wt%Al磁粉(20.0 g,长沙天久金属材料有限公司)混合均匀后,分散于上述NaNO3溶液中,并在25 ℃下持续搅拌10 min。将钝化后的磁粉在无水乙醇(国药集团有限公司)中清洗,并在80 ℃下真空干燥,然后与润滑剂硬脂酸锌(0.5wt%,上海麦克林生化科技有限公司)混合。混合后的粉末在1900 MPa的压强下成型,获得环形软磁复合材料(外径为23.6 mm,内径为14.4 mm,厚度为7.0 mm)。最后,将软磁复合材料在氩气保护下,于700 ℃退火1 h以去除内应力。
利用扫描电子显微镜(SEM, Hitachi S-4800)观察磁粉形貌,并通过傅里叶变换红外光谱仪(FTIR, Nicolet 5700)和X射线光电子能谱仪(XPS, ESCALAB 250Xi)研究包覆层的化学结构。采用配备选区电子衍射(SAED)和能量色散X射线光谱(EDS)的透射电子显微镜(TEM, Titan G2 80-200, FEI)对包覆层的成分和微观结构进行表征。图S1为聚焦离子束(FIB)切割磁粉制备透射电镜样品方法。软磁复合材料的密度及孔隙率通过阿基米德排水法测量,计算过程详见补充材料。利用四探针电阻测试仪测量复合材料的电阻率,并采用软磁自动测量系统(MATS-2010SA)测试磁环在外加磁场为100 mT、频率范围为25~175 kHz下的有效磁导率与损耗。
《3、 结果与讨论》
3、 结果与讨论
《3.1 软磁复合材料的磁性能》
3.1 软磁复合材料的磁性能
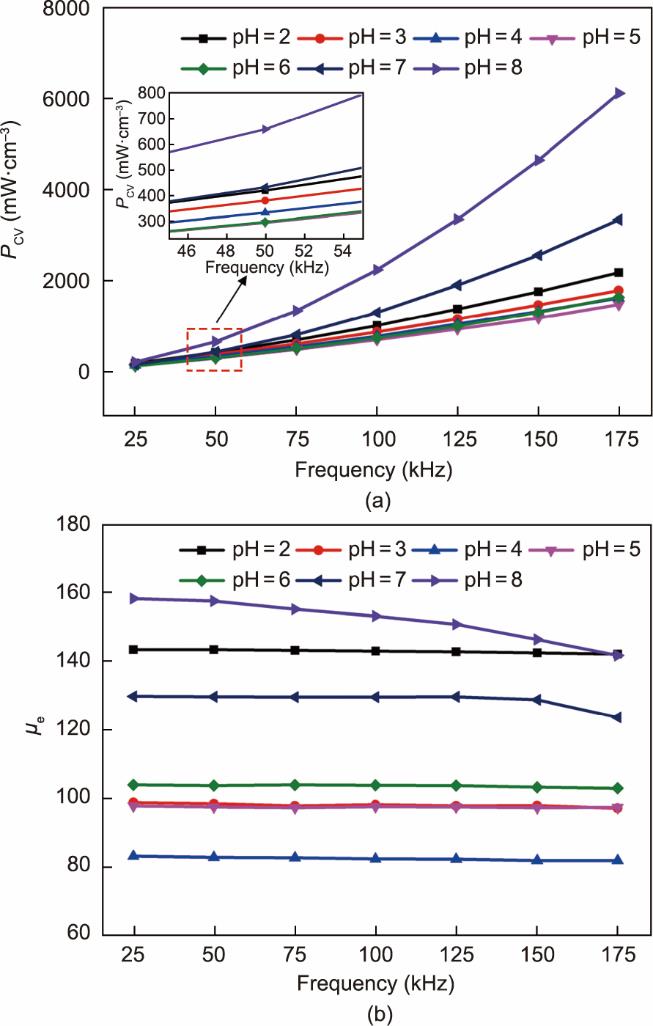
附录A中的图S2为NaNO3钝化液浓度从10wt%增至30wt%时,对软磁复合材料损耗Pcv和有效磁导率μe的作用规律。由于形成薄且完整的包覆层,因此20wt% NaNO3钝化综合性能最优。采用CH3COOH/CH3COONa缓冲液调节20wt%浓度NaNO3溶液的pH值。图1为NaNO3钝化液的pH值为2~8时对软磁复合材料Pcv和μe的影响。频率50 kHz条件下的损耗和磁导率,以及样品的密度、孔隙率和电阻率的具体数据总结于表1。如图1中插图所示,随着钝化液pH值的升高,软磁复合材料的Pcv逐渐降低,pH为5时损耗最低(296.4 mW∙cm-3),之后Pcv随pH值增加而上升,pH=8时损耗上升至660.2 mW∙cm-3。随着pH从2增至4,μe从143.4减少至82.5 [图1(b)]。进一步提高钝化液pH值,μe单调上升,且pH=8时,μe增加至157.6。综上,当钝化液pH=5时,可获得最优综合性能(Pcv=296.4 mW∙cm-3, μe=97.6)。上述磁性能的演变将在下文中具体讨论。附录A中的表S1对比了本工作与文献中其他包覆方法制备FeSiAl SMCs的损耗和磁导率,可见通过本方法制备的SMCs表现出更为优异的综合交流磁性能。
《图1》
图1 不同pH时20wt% NaNO3溶液钝化样品的损耗(a)和有效磁导率(b)随频率变化。
《表1》
表1 软磁复合材料的损耗、磁导率、密度、孔隙率及电阻率
| pH values | Density (g∙cm-3) | Porosity (%) | Electrical resistivity (Ω∙cm) | ||
|---|---|---|---|---|---|
| 2 | 421.4 | 143.4 | 6.17 | 7.84 | 0.96 |
| 3 | 382.4 | 98.2 | 6.11 | 8.41 | 2.12 |
| 4 | 335.7 | 82.5 | 6.01 | 9.22 | 5.21 |
| 5 | 296.4 | 97.2 | 6.10 | 8.36 | 8.23 |
| 6 | 299.1 | 103.5 | 6.13 | 8.12 | 7.86 |
| 7 | 433.9 | 129.6 | 6.16 | 7.49 | 4.52 |
| 8 | 660.2 | 157.6 | 6.21 | 6.58 | 0.16 |
《3.2 绝缘包覆层表征》
3.2 绝缘包覆层表征
图2为pH=2、5和8时NaNO3溶液钝化后FeSiAl磁粉的SEM图像。在pH=2时,可能由于过度反应使样品表面形成的包覆层不连续[图2(a)、(b)]。在pH=5时,磁粉表面相对光滑[图2(c)],如图2(d)的放大图所示,形成了均匀的包覆层。进一步提高pH值至8时,由图2(e)中选取的矩形区域放大图[图2(f)]可见,磁粉表面绝缘包覆不完整。
《图2》
图2 FeSiAl磁粉经pH=2 [(a)、(b)]、pH=5 [(c)、(d)]及pH=8 [(e)、(f)]的NaNO3溶液钝化后的SEM图像。(b)、(d)和(f)分别为(a)、(c)和(e)中矩形区域的放大图。
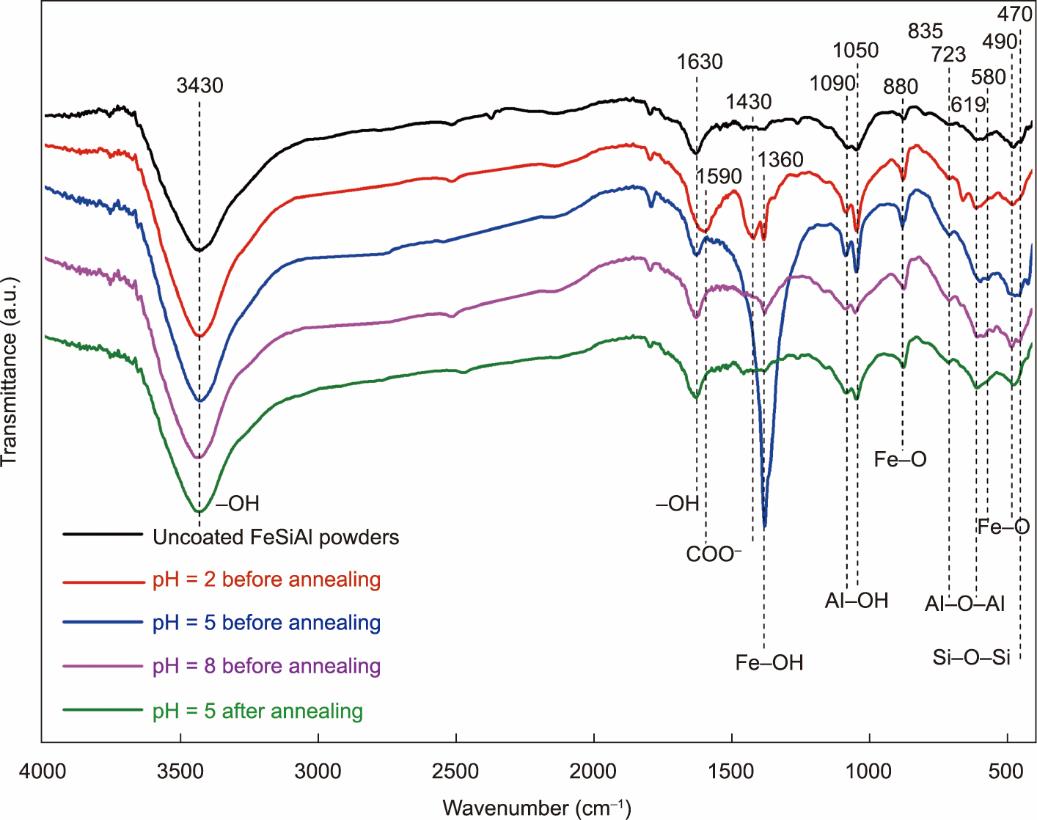
为了揭示不同pH下包覆层的演变规律,对钝化前后的FeSiAl磁粉进行了FTIR测试(图3)。所有样品均在1630 cm-1和3430 cm-1附近出现强吸收峰,对应于吸附水分子的伸缩振动[14]。对于未包覆的FeSiAl磁粉,470 cm-1处的吸收峰源于Si‒O‒Si的伸缩振动[15],而490 cm-1和580 cm-1对应于Fe‒O的振动峰[16‒17],723 cm-1和619 cm-1的吸收峰分别对应于Al‒O‒Al和Al‒O的伸缩振动[18]。Fe‒O、Al‒O和Si‒O基团的存在表明原磁粉存在一定程度的表面氧化。钝化液pH=2时,由于酸性溶液中CH3COOH的浓度较高,1430 cm-1和1590 cm-1处额外的吸收峰分别对应于COO‒离子的非对称和对称伸缩振动[19‒20]。此外,在1360 cm‒1处出现Fe‒OH的吸收峰[21‒22],且在1050 cm‒1和1090 cm‒1处观察到Al‒OH的吸收峰[23‒25]。当NaNO3溶液的pH值增至5时,由于氢氧化物[如Fe(OH)3和Al(OH)3]沉淀[26‒28],Fe‒OH吸收峰强度显著增强,Al‒OH峰强度略为增加。当pH=8时,对应于Fe‒OH的吸收峰几乎消失,这是因为Fe在碱性条件下几乎不与NO3-反应,且Al‒OH的吸收峰相对较弱,说明生成的包覆层很薄。在pH=5时制备的样品经700 ℃退火后,Fe‒OH的吸收峰几乎消失不见,而723 cm-1、619 cm-1、580 cm-1及490 cm-1处的Al‒O和Fe‒O峰明显增强,表明退火过程中氢氧化物分解形成相应的氧化物,而残余Al‒OH吸收峰的存在说明氢氧化铝退火时部分分解。
《图3》
图3 未包覆FeSiAl磁粉和不同pH下20wt% NaNO3钝化磁粉退火前后的FTIR图谱。
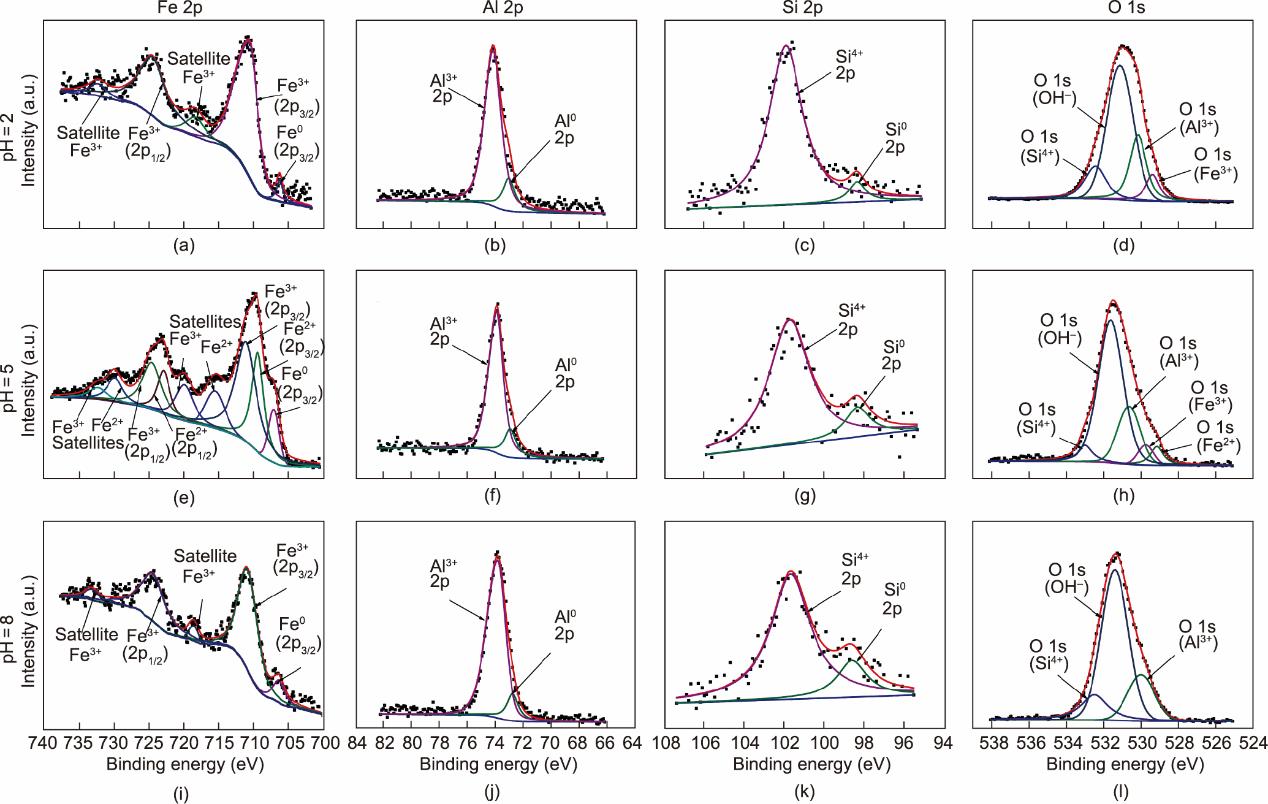
对不同pH值下钝化并经700 ℃退火的样品进行XPS表征,附录A中的图S3为所有样品Fe、Al、Si和O元素的全谱扫描结果。由于Al元素的反应活性,其在包覆层中占据相当比例。随着pH增加,Fe2p峰的相对强度降低,而Al2p峰强度增加,表明Fe在碱性环境中难以被氧化,Al则相反。图4(a)为pH=2时钝化样品的Fe2p谱,其包含Fe0 (706.2 eV)和Fe3+ (710.7 eV)峰[29‒30],且在718.3 eV和732.4 eV处出现Fe2O3的特征卫星峰[31]。图4(b)中可以观察到Al3+ (74.3 eV)和Al0 (72.9 eV)两个主要的峰[32],Fe0和Al0峰的存在说明包覆层很薄。图4(c)为Si2p图谱,包含Si0 (98.4 eV)和Si4+ (102.1 eV)峰,对应于Si单质和SiO2 [33‒34]。图4(d)中的O1s峰可由位于529.4 eV、530.3 eV、531.2 eV和532.5 eV的四个分峰拟合而成,分别对应于Fe3+、Al3+、OH‒及Si4+ [31‒33]。因此,pH=2时NaNO3溶液钝化形成的包覆层主要由Fe2O3、Al2O3、SiO2及氢氧化物组成。
《图4》
图4 FeSiAl磁粉在pH为2、5和8的NaNO3溶液中钝化并退火后的Fe2p [(a)、(e)、(i)]、Al2p [(b)、(f)、(j)]、Si2p [(c)、(g)、(k)]及O1s [(d)、(h)、(l)] XPS图谱。
当pH增至5时,如图4(e)所示,Fe2p图谱由Fe0 (706.9eV)、Fe2+ (709.2eV)和Fe3+ (710.9eV)峰组成。其中Fe2+与Fe3+的比例小于1∶2,表明包覆层中同时存在Fe2O3和Fe3O4。图4(f)中的Al2p图谱包含Al3+和Al0峰,且图4(g)中的Si2p图谱包含Si4+和Si0峰。图4(h)中的O1s图谱需要由位于529.1 eV、529.9 eV、530.8 eV、531.7 eV和532.7 eV的五个分峰进行拟合,分别对应于Fe2+、Fe3+、Al3+、OH‒和Si4+。因此,pH=2时NaNO3溶液钝化形成的包覆层主要由Fe2O3、Fe3O4、Al2O3、SiO2及氢氧化物组成。
当pH=8时,钝化后磁粉的Fe2p图谱中含有Fe0峰和微弱的Fe3+峰[图4(i)]。图4(j)中的Al2p图谱可分为Al3+和Al0峰。图4(k)中的Si2p图谱包含Si4+和Si0,且Si2p峰位向低结合能方向移动,从102.1 eV降为101.6 eV,这与已有结果[35]一致,表明Si的反应速率随着pH值增加而降低。O1s图谱拟合结果说明存在OH-、Al3+、Fe3+及Fe2+。因此,pH=2时NaNO3溶液钝化形成的包覆层主要由Al2O3、SiO2和氢氧化物组成。
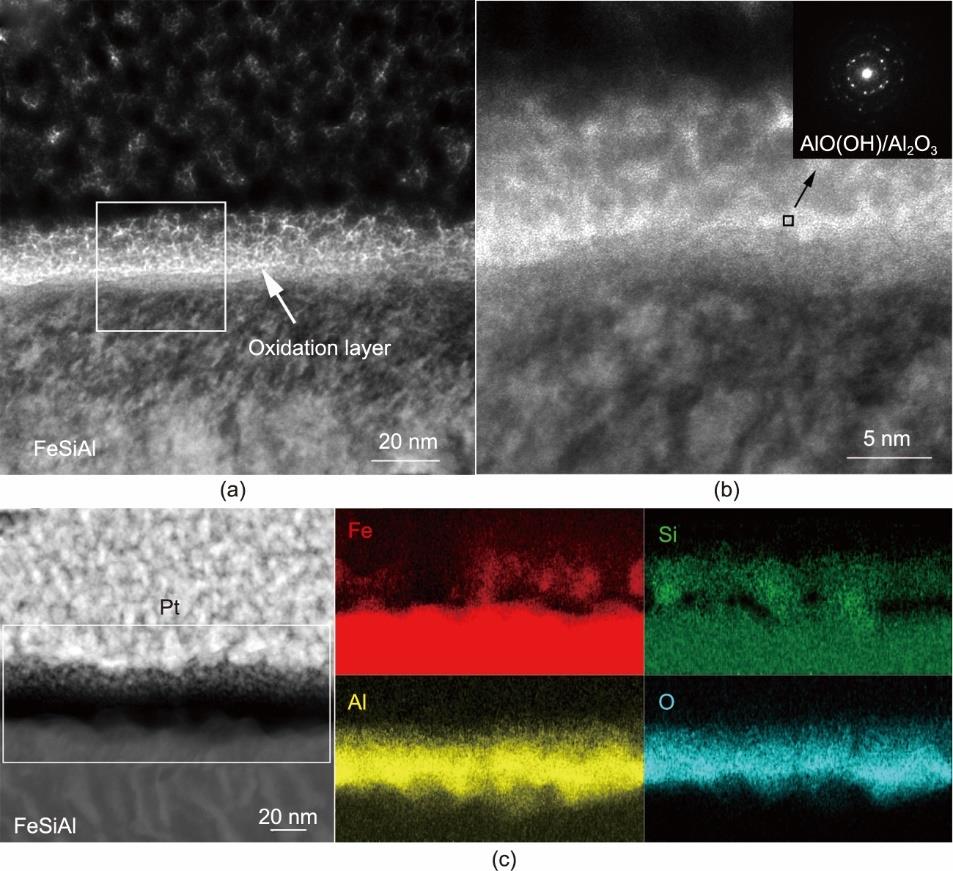
图5为FeSiAl磁粉经pH=2的NaNO3钝化且退火后包覆层截面的TEM图像。包覆层由图5(a)中箭头所示,可以观察到双层包覆结构,厚度为(8.6±0.5) nm。图5(b)中的插图为图5(a)中矩形区域的SAED图,表包覆层中非晶与晶态结构共存。其中,衍射环的间距(2.81 Å)对应于AlO(OH) [36‒37]。结合前文FTIR及XPS分析,衍射斑点可能对应于700 ℃退火后AlO(OH)部分分解形成的晶态Al2O3 [38‒39]。图5(c)为包覆层和磁粉基体的高角环形暗场(HAADF)图像及在选取的矩形区域中不同元素的EDS面扫图,表明包覆层中Fe、Si、Al和O元素共存。综上,包覆层主要含有Fe2O3、SiO2、Al2O3和AlO(OH)。
《图5》
图5 FeSiAl磁粉在pH=2的NaNO3钝化液中钝化并退火后截面的TEM图像(a)和选取矩形区域得到的SAED图(b);(c)HAADF图像及在选取矩形区域得到的Fe、Si、Al、O元素的EDS元素分布。
图6(a)为在pH=5时钝化样品的截面TEM图像。如箭头所示的包覆层显示出厚度为(11.2±0.3) nm的双层结构。根据图6(b)插图中的SAED图可知,包覆层中同时含有晶态Al2O3和非晶AlO(OH),而图6(c)中的HAADF图像和EDS面扫结果表明包覆层中主要包含Al和O,还有少量的Fe和Si元素。
《图6》
图6 FeSiAl磁粉在pH=5的NaNO3钝化液中钝化并退火后截面的TEM图像(a)和选取矩形区域得到的SAED图(b);(c)HAADF图像及在选取矩形区域得到的Fe、Si、Al、O的EDS元素分布。
为了揭示碱性条件的影响,本文还研究了pH=8时NaNO3钝化且退火后磁粉包覆层的微观结构和成分。由图7(a)可见,磁粉基体和包覆层之间存在波浪形的界面,且通过对不同区域获得的多张TEM图像测量得到包覆层的平均厚度仅为(6.7±0.8) nm。图7(b)中更高放大倍数的TEM以及SAED图表明包覆层中非晶AlO(OH)和晶态Al2O3共存。图7(c)所示的HAADF和EDS结果表明包覆层的主要成分为Al、Si和O。综上,pH=8条件下钝化样品退火后形成了厚度较薄,且主要包含Al2O3、AlO(OH)和SiO2的包覆层。
《图7》
图7 FeSiAl磁粉在pH =8的NaNO3钝化液中钝化并退火后截面的TEM图像(a)和选取矩形区域得到的SAED图(b);(c)HAADF图像及在选取矩形区域得到的Fe、Si、Al、O的EDS元素分布。
《3.3 绝缘包覆层生长机理》
3.3 绝缘包覆层生长机理
图8为FeSiAl磁粉表面具有阻挡层和沉淀层双层结构的包覆层生长模型[40]。在钝化过程中,部分Fe、Al和Si原子被直接氧化为Fe2O3、Fe3O4、Al2O3和SiO2,形成内层的氧化物阻挡层。Fe3+和Al3+等阳离子可以穿过阻挡层,在阻挡层和NaNO3溶液之间的界面处以水解沉淀的方式形成由Fe(OH)3、Al(OH)3和AlO(OH)组成的外层沉淀层。
《图8》
图8 FeSiAl磁粉表面双层结构包覆层生长示意图。
当pH=2时,阻挡层由Fe、Al和Si通过反应(1)~(3)氧化而形成。反应的吉布斯自由能
(1)
(2)
(3)
Al和Si在pH=5条件下的氧化反应与pH=2时的反应相似。然而,由于NO3-的氧化性随着H+浓度的降低而减弱,Fe的氧化反应发生如下变化,导致Fe2+和Fe3+共存。此外,由于H+浓度的降低,所沉淀氢氧化物的溶解减少。
(4)
进一步将pH提高至8,由于NO3-的氧化性不足,Fe不发生氧化反应,钝化反应受到阻碍。此外,反应(2)和(3)的进行程度降低导致水解沉淀减慢,同时沉淀物几乎不会发生溶解。在碱性NaNO3溶液中,FeSiAl粉末表面可能通过以下反应发生局部腐蚀[图2(e)]:
(5)
阻挡层和沉淀层形成的动力学过程可以根据点缺陷模型进行解释[43]。阻挡层的生长主要由金属和阻挡层之间界面处的反应(6)决定,其溶解取决于阻挡层和沉淀层之间界面上的反应(7)。
(6)
(7)
式中,m和MM分别是金属原子和金属阳离子;VO是氧空位;MO
(8)
式中,L是随时间t变化的阻挡层的厚度;Ω是阻挡层中阳离子的摩尔体积;
(9)
式中,
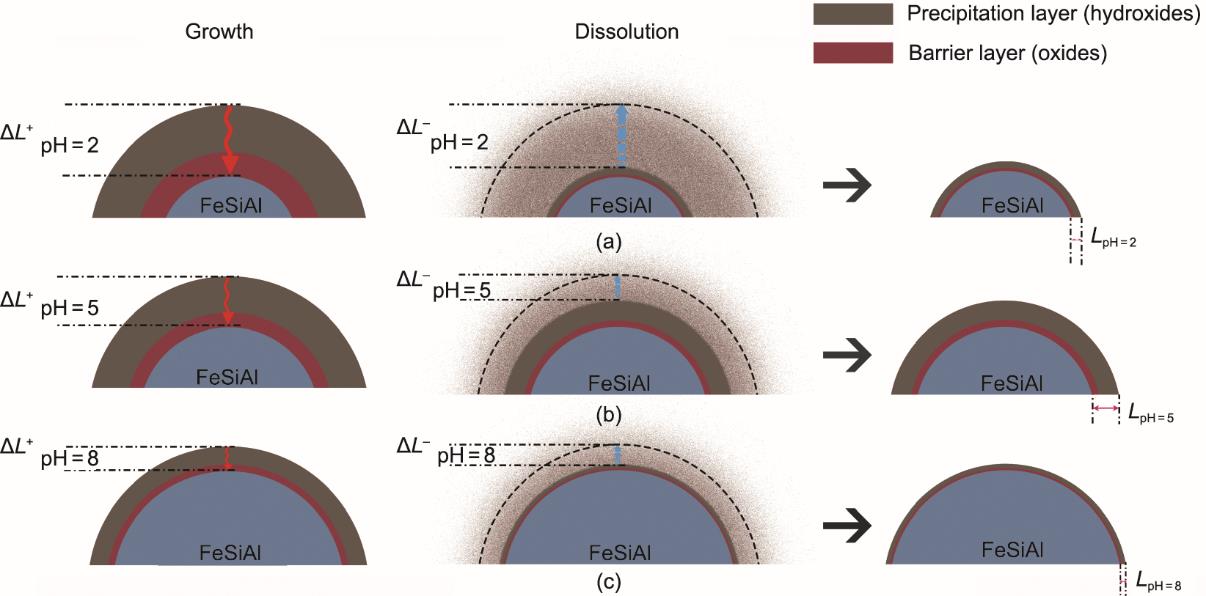
图9展示了不同pH值下包覆层的演变规律。当pH=2时,由于H+浓度较高,
《图9》
图9 在pH为2(a)、5(b)和8(c)时钝化层的生长和溶解过程示意图。
《3.4 绝缘包覆与磁性能关联机制》
3.4 绝缘包覆与磁性能关联机制
根据上述包覆层形成机制,可对图1中软磁复合材料的性能演变机制进行分析。当pH值从2增加至5时,含有大量非磁性相的绝缘包覆层厚度增加,对畴壁产生钉扎,导致μe减小。在pH值为8时,包覆层厚度小且不完整,使涡流损耗增加且引起趋肤效应[45],μe表现出较差的频率稳定性。
软磁复合材料的损耗由磁滞损耗Ph、涡流损耗Pe和剩余损耗Pr组成。其中,剩余损耗仅在低场高频下发挥主要作用,在本工作中可忽略不计。因此,可以根据下式对Pcv进行分离[46]:
(10)
式中,k1和k2为磁滞损耗系数和涡流损耗系数;f为频率。图10为在不同pH值下制备磁芯的Ph和Pe对总损耗的贡献。Ph主要取决于矫顽力,当pH值从2增加至5时,由于包覆层厚度增加,畴壁的钉扎位点增多而导致矫顽力和磁滞损耗增加。pH值为8时生成的包覆层薄且不完整,Ph随之下降。Pe取决于样品的电阻率,在pH=5时可以形成具有足够厚度且包覆完整的绝缘层,电阻率显著提高,具有最低的涡流损耗。
《图10》
图10 不同pH条件下制备的磁芯总损耗Pcv分离为涡流损耗Pe和磁滞损耗Ph的情况。
《4、 结论》
4、 结论
本工作发明NaNO3钝化新绝缘包覆技术制备FeSiAl SMCs。基于微观结构和成分分析,揭示了包覆层在不同pH条件下的演变规律,并通过详尽的热力学和动力学分析明确了包覆层的生长机理。通过优化NaNO3钝化液的pH值,FeSiAl SMCs获得了最佳综合磁性能(μe=97.2, Pcv=296.4 mW∙cm-3)。本工作发明的NaNO3钝化技术不仅可以扩展用于其他软磁合金体系,亦为开发利用氧化性物质如亚硝酸盐、超氧化物和高锰酸盐等制备新型绝缘包覆层奠定了基础。


















 京公网安备 11010502051620号
京公网安备 11010502051620号




